
”¾ĢāÄæ”æČżŃõ»Æøõ£ØCrO3£©³£ÓĆÓŚ½šŹō¶Ęøõ”£¹¤ŅµÉĻÖĘŌģČżŃõ»ÆøõµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗX£«H2SO4£½2CrO3£«Na2SO4£«H2O£¬ĘäÖŠXµÄ»ÆѧŹ½ŹĒ
A. Na2CrO4 B. Na2Cr2O7 C. Na2Cr2O4 D. Na2CrO7

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøÖÖĘ¹¹¼žŌŚ¶ĘŠæĒ°ŠčŅŖ¾¹żĖįĻ“£¬Ę仳±¾ŌĄķŹĒÓĆŃĪĖį³żČ„Ęä±ķĆęµÄFe2O3”¤H2O¼°FeOµČŌÓÖŹ”£»ŲŹÕ·ĻĖįĶ¬Ź±Éś²śŗ¬Ģś²śĘ·µÄĮ÷³ĢČēĻĀ£ŗ

ŅŃÖŖ£ŗ
i£®ĖįĻ“øÖÖĘ¹¹¼žŗóµĆµ½·ĻĖįµÄÖ÷ŅŖ³É·ÖČēĻĀ±ķĖłŹ¾”£

ii.pH <4Ź±£¬Fe2+²»Ņ×±»ŃõĘųŃõ»Æ”£
£Ø1£©ÓĆĄė×Ó·½³ĢŹ½½āŹĶ·ĻĖįÖŠ²»ŗ¬Fe3+µÄŌŅņ______________________________”£
£Ø2£©¹ż³ĢIIÖŠ£¬·¢ÉśµÄÖ÷ŅŖ·“Ó¦£ŗFeCl2(s)Ź®H2SO4(aq) ![]() FeSO4(s)+2HCl( aq)”£
FeSO4(s)+2HCl( aq)ӣ
¢Ł¼ÓČė¹żĮæH2SO4µÄ×÷ÓĆŹĒ__________________________________£ØŠ“³öŅ»µć¼“æÉ£©”£
¢ŚÓĆ»ÆŃ§Ę½ŗāŌĄķ½āŹĶ¹ÄČėæÕĘųµÄÄæµÄ£ŗ_________________________________”£
£Ø3£©¹ż³ĢIIIÖŠ£¬FeSO4øō¾ųæÕĘų±ŗÉÕµĆµ½µÄĪ²ĘųÖŠŗ¬ÓŠĮ½ÖÖæÉÓĆÓŚÉś²śĮņĖįµÄŃõ»ÆĪļ£¬“Ė¹ż³Ģ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________________________________”£
£Ø4£©¹ż³ĢV:ŅõĄė×Ó½»»»Ź÷Ö¬æɽ«FeCl4-Ń”ŌńŠŌĪüø½·ÖĄė£¬Ęä¹ż³ĢæɱķŹ¾ĪŖROH +X-![]() RX +OH-£ØX-±ķŹ¾FeCl4-£©”£µ±Ź÷Ö¬Īüø½±„ŗĶŗóæÉÖ±½ÓÓĆĖ®Ļ“µÓŹ÷Ö¬½ųŠŠĶŃø½£¬Ķ¬Ź±ĶŃø½¹ż³Ģ·¢Éś·“Ó¦£ŗFeCl4-
RX +OH-£ØX-±ķŹ¾FeCl4-£©”£µ±Ź÷Ö¬Īüø½±„ŗĶŗóæÉÖ±½ÓÓĆĖ®Ļ“µÓŹ÷Ö¬½ųŠŠĶŃø½£¬Ķ¬Ź±ĶŃø½¹ż³Ģ·¢Éś·“Ó¦£ŗFeCl4-![]() Fe3+ +4C1-”£
Fe3+ +4C1-ӣ
¢ŁĪüø½ŗóČÜŅŗµÄpH½«»į_______________”££ØĢī”°Éżøß”±”¢”°½µµĶ”±»ņ”°²»±ä”±£©
¢ŚĻ“ĶŃŅŗ¾“¦ĄķŗóÓŠŠķ¶ąÓĆĶ¾£¬ĻĀĮŠÓĆĶ¾ŗĻĄķµÄŹĒ_________________”£
A”¢æĢŹ“Ó”Ė¢ĶĻßĀ·°å B”¢¾»»ÆĪŪĖ® C”¢×ŌĄ“Ė®Ļū¶¾ D”¢½žÅŻÉśĪļ±ź±¾
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCOŹĒĻÖ“ś»Æ¹¤Éś²śµÄ»ł“”ŌĮĻ£¬ĻĀĮŠÓŠ¹ŲĪŹĢā¶¼ŗĶCOµÄŹ¹ÓĆÓŠ¹Ų”£
£Ø1£© ĄūÓĆCOÉś²śŅŅ“¼: 2CO£Øg£©£«4H2£Øg£©![]() CH3CH2OH£Øg£©£«H2O£Øg£© ¦¤H1
CH3CH2OH£Øg£©£«H2O£Øg£© ¦¤H1
ÓÖŅŃÖŖ£ŗH2O£Øl£©=== H2O£Øg£©¦¤H2 CO£Øg£©£«H2O£Øg£©![]() CO2£Øg£©£«H2£Øg£© ¦¤H3
CO2£Øg£©£«H2£Øg£© ¦¤H3
¹¤ŅµÉĻŅ²æÉĄūÓĆCO2£Øg£©ÓėH2£Øg£©ĪŖŌĮĻŗĻ³ÉŅŅ“¼£ŗ2CO2£Øg£©£«6H2£Øg£©![]() CH3CH2OH£Øg£©£«3H2O£Øl£© ¦¤H
CH3CH2OH£Øg£©£«3H2O£Øl£© ¦¤H
Ōņ£ŗ¦¤HÓė¦¤H1”¢¦¤H2”¢¦¤H3Ö®¼äµÄ¹ŲĻµŹĒ£ŗ¦¤H£½_______________________”£
£Ø2£©Ņ»¶ØĢõ¼žĻĀ£¬H2”¢COŌŚĢå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗ4H2£Øg£©+2CO£Øg£©![]() CH3OCH3£Øg£©+H2O£Øg£©£¬
CH3OCH3£Øg£©+H2O£Øg£©£¬
ĻĀĮŠ“ėŹ©ÖŠÄܹ»Ķ¬Ź±Āś×ćŌö“ó·“Ó¦ĖŁĀŹŗĶĢįøßCO×Ŗ»ÆĀŹµÄŹĒ________£ØĢī×ÖÄø£©”£
A.Ź¹ÓĆøߊ§“߻ƼĮ B£®½µµĶ·“Ó¦ĪĀ¶Č
C.Ōö“óĢåĻµŃ¹Ēæ D£®²»¶Ļ½«CH3OH“Ó·“Ó¦»ģŗĻĪļÖŠ·ÖĄė³öĄ“
£Ø3£©²ÉÓĆCOÓėH2·“Ó¦ŗĻ³ÉŌŁÉśÄÜŌ“¼×“¼£¬·“Ó¦ČēĻĀ:
CO£Øg£©+ 2H2£Øg£©![]() CH3OH£Øg£©
CH3OH£Øg£©
ŌŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äÓŠ10molCOŗĶ20mol H2£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ӧɜ³É¼×“¼”£COµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£Øp£©µÄ¹ŲĻµČē£ØĶ¼1£©ĖłŹ¾”£
¢ŁŗĻ³É¼×“¼µÄ·“Ó¦ĪŖ______£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©·“Ó¦”£
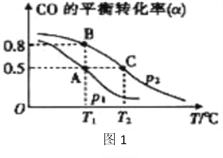
¢ŚA”¢B”¢CČżµćµÄĘ½ŗā³£ŹżKA”¢KB”¢KCµÄ“󊔹ŲĻµĪŖ__________”£
¢ŪČō“ļµ½Ę½ŗāדĢ¬AŹ±£¬ČŻĘ÷µÄĢå»żĪŖ10L£¬ŌņŌŚĘ½ŗāדĢ¬BŹ±ČŻĘ÷µÄĢå»żĪŖ_______________L”£
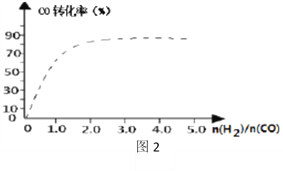
¢Ü£ØĶ¼2£©ÖŠŠéĻßĪŖøĆ·“Ó¦ŌŚŹ¹ÓĆ“ß»Æ¼ĮĢõ¼žĻĀ¹ŲÓŚĘšŹ¼ĒāĘųÓėCOĶ¶ĮĻ±ČŗĶCOĘ½ŗā×Ŗ»ÆĀŹµÄ¹ŲĻµĶ¼”£µ±ĘäĢõ¼žĶźČ«ĻąĶ¬Ź±£¬ÓĆŹµĻß»³ö²»Ź¹ÓĆ“ß»Æ¼ĮĒéæöĻĀCOĘ½ŗā×Ŗ»ÆĀŹµÄŹ¾ŅāĶ¼£®____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢Z”¢WµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£XŌ×Ó×īĶā²ć±Č“ĪĶā²ć¶ą3øöµē×Ó;Y”¢Z¾łĪŖ½šŹō,YŹĒĶ¬ÖÜĘŚÖŠŌ×Ó°ė¾¶×ī“óµÄŌŖĖŲ,ZµÄ¼ņµ„Ąė×Ó°ė¾¶ŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īŠ”;WµÄ×īøß¼ŪŃõ»ÆĪļŌŚĪŽ»śŗ¬ŃõĖįÖŠĖįŠŌ×īĒ攣ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. XµÄĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČŃõµÄĒæ
B. ŌŖĖŲZ”¢WµÄ¼ņµ„Ąė×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹
C. Y”¢Z”¢WµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÖ®¼äÄÜĻą»„·“Ó¦
D. µČÖŹĮæµÄYŗĶZµ„ÖŹ·Ö±šÓė×ćĮæĻ”ŃĪĖį·“Ó¦,Ē°Õß²śÉśµÄĒāĘų¶ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń. Īų»ÆŠæŹĒŅ»ÖÖĶøĆ÷°ėµ¼Ģå,Ņ²æÉ×÷ĪŖŗģĶā¹āѧ²ÄĮĻ,ČŪµćŹĒ1 520 ”ę”£
£Ø1£©»łĢ¬ŠæŌ×ӵļŪµē×ÓÅŲ¼Ź½ŹĒ_______”£
£Ø2£©øł¾ŻŌŖĖŲÖÜĘŚĀÉ,µēøŗŠŌSe____S,µŚŅ»µēĄėÄÜSe____As(Ģī”°>”±»ņ”°<”±)”£
£Ø3£©H2SeµÄ·Ö×Ó¹¹ŠĶŹĒ____,ĘäÖŠĪųŌ×ÓµÄŌӻƹģµĄĄąŠĶŹĒ____”£
£Ø4£©H2OµÄ·ŠµćøßÓŚH2SeµÄ·Šµć(-42 ”ę),ĘäŌŅņŹĒ________________”£
£Ø5£©¾§ĢåZnĪŖĮł·½×īĆܶѻż,ĘäÅäĪ»ŹżŹĒ____”£
¢ņ µŖ¼°Ęä»ÆŗĻĪļÓėČĖĄąÉś²ś”¢Éś»īĻ¢Ļ¢Ļą¹Ų”£»Ų“šĻĀĮŠĪŹĢā:
£Ø1£©C”¢N”¢OČżÖÖŌŖĖŲµŚŅ»µēĄėÄܓӓ󵽊”µÄĖ³ŠņŹĒ________”£
£Ø2£©1 mol N2F2ŗ¬ÓŠ____ mol ¦Ņ¼ü”£
£Ø3£©NH4BF4(·śÅšĖįļ§)ŹĒŗĻ³ÉµŖ»ÆÅšÄÉĆ׹ܵÄŌĮĻÖ®Ņ»”£1 mol NH4BF4ŗ¬____ molÅäĪ»¼ü”£
£Ø4£©°²Č«ĘųÄŅ“ņæŖŹ±·¢ÉśµÄ»Æѧ·“Ó¦ĪŖ10NaN3+2KNO3 = K2O+5Na2O+16N2”ü”£
¢ŁŠ“³öÓėN2»„ĪŖµČµē×ÓĢåµÄ·Ö×Ó________”£
¢ŚNa2OµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾,¾§°ū±ß³¤ĪŖ566 pm,¾§°ūÖŠŃõŌ×ÓµÄÅäĪ»ŹżĪŖ____,Na2O¾§ĢåµÄĆܶČĪŖ______(Ö»ŅŖĒóĮŠĖćŹ½,²»±Ų¼ĘĖć³ö½į¹ū)£¬Na+ ÓėO2£¼äµÄ×ī¶Ģ¾ąĄėĪŖ_____pm”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ 38.4gĶøśŹŹĮæµÄÅØĻõĖį·“Ó¦£¬ĶĶźČ«×÷ÓĆŗ󣬹²ŹÕ¼Æµ½ĘųĢå22.4L£Ø±ź×¼×“æö£©£¬·“Ó¦ĻūŗĵÄHNO3µÄĪļÖŹµÄĮææÉÄÜŹĒ
A£®1.0molB£®1.6 molC£®2.2 mol D£®2.4 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ1L 2 mol/L Na2SO4ČÜŅŗÖŠĖłŗ¬µÄNa+ĪļÖŹµÄĮæĪŖ ( )
A. 2mol B. 4mol C. 1mol D. 0.5mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌŌöÉśŠŌń£ŗŪŌēĘŚ½ųŠŠ ![]() Sr£ØļČ£©øÉŌ¤æÉČ”µĆ½ĻŗĆŠ§¹ū£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
Sr£ØļČ£©øÉŌ¤æÉČ”µĆ½ĻŗĆŠ§¹ū£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.SrĪŖÓŚµŚ4ÖÜĘŚ¢ņA ×å
B.![]() SrŗĖÄŚÖŠ×ÓŹżÓėÖŹ×ÓŹżÖ®²īĪŖ14
SrŗĖÄŚÖŠ×ÓŹżÓėÖŹ×ÓŹżÖ®²īĪŖ14
C.![]() SrÓė
SrÓė ![]() Y»„ĪŖĶ¬Ī»ĖŲ
Y»„ĪŖĶ¬Ī»ĖŲ
D.![]() SrµÄŗĖÄŚÖŹ×ÓŹżĪŖ38£¬SrŌŖĖŲµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ90
SrµÄŗĖÄŚÖŹ×ÓŹżĪŖ38£¬SrŌŖĖŲµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ90
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬ŌŚĶŠæŌµē³ŲÖŠ£¬ŅŌĻ”ĮņĖįĪŖµē½āÖŹČÜŅŗ£ŗ 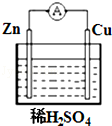
£Ø1£©ŠæʬĪŖ¼«£¬µē¼«ÉĻ·¢Éś·“Ó¦£®£Ø”°Ńõ»Æ”±»ņ”°»¹Ō”±£©
£Ø2£©µē¼«·“Ó¦Ź½£ŗ
£Ø3£©ŠæʬÉĻ¹Ū²ģµ½µÄĻÖĻó£ŗ
£Ø4£©ĶʬĪŖ¼«£¬µē¼«ÉĻ·¢Éś·“Ó¦£®£Ø”°Ńõ»Æ”±»ņ”°»¹Ō”±£©
£Ø5£©µē¼«·“Ó¦Ź½£ŗ
£Ø6£©ĶʬÉĻ¹Ū²ģµ½µÄĻÖĻó£ŗ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com