
【题目】根据所学物质分类知识,回答下列问题。有下列10种物质
①CH3CH2CH3 ②CH2==CH2 ③![]() ④
④ ![]() ⑤CH3CH2CH2OH ⑥CH3CHO ⑦CuSO4·5H2O ⑧Fe ⑨CH3COOH ⑩CH3COONa
⑤CH3CH2CH2OH ⑥CH3CHO ⑦CuSO4·5H2O ⑧Fe ⑨CH3COOH ⑩CH3COONa
(1)属于无机化合物的是 _______。
(2)属于烃的是_______。
(3)属于烷烃的是______,属于酸的是______。
(4)属于有机化合物的是_______ 。属于烃的衍生物的是_______ 。
科目:高中化学 来源: 题型:
【题目】下列关于铜锌原电池(稀硫酸作电解质溶液)的叙述错误的是( )
A.电子由正极通过导线流向负极
B.负极反应式为:Zn﹣2e﹣=Zn2+
C.正极产生1molH2电池转移2mol电子
D.可以用碳棒代替铜片作为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】借助下表提供的信息,实验室制备乙酸丁酯所采取的措施正确的是
物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 |
沸点 | 117.9℃ | 117.2℃ | 126.3℃ |
A. 采用水浴加热 B. 使用浓硫酸做催化剂
C. 用NaOH(aq)洗涤产物后分液 D. 边制备边蒸出乙酸丁酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组在实验室利用直接合成法制各甘氨酸亚铁。有关物质性质如下所示:
甘氨酸( NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇、 | 易溶于水和乙醇, | 易溶于水, |
两性化合物 | 有强酸性和还原性 | 难溶于乙醇 |
实验过程及装置图如下(夹持和加热仪器已省略):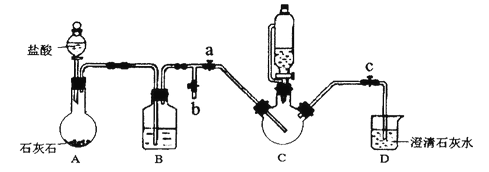
I.合成:在C中加入0.10mol甘氨酸、0.05mol硫酸亚铁、少量柠檬酸和200mL水,利用CO2将C装置中的空气排净,然后在40℃恒温条件下用磁力搅拌器不断搅拌,并用恒压滴液漏斗向C中滴加6mol·L-1NaOH溶液调节pH到6左右,使反应物充分反应。
II.分离:加入无水乙醇,立即出现白色沉淀。将沉淀进行过滤、洗涤,收集滤渣。
Ⅲ.提纯:将滤渣溶解于适量的蒸馏水中,然后结晶、过滤,将纯化后的产品放入真空干燥箱中干燥后称重。
回答下列问题:
(1)B装置的作用是______________;
(2)能证明C装置中空气排净的现象是______________;向C中滴加NaOH溶液之前应该停止滴加盐酸,且关闭止水夹____________,打开止水夹________
(3)“合成”中加入柠檬酸的作用是______________:请写出合成甘氨酸亚铁的化学方程式_________。
(4)加入乙醇的目的是________;“提纯”时用的结晶方法为________________
(5)通过测量得知:等浓度(NH2CH2COO)2Fe 溶液导电能力远小于FeSO4溶液。暴露在空气中,(NH2CH2COO)2Fe溶液比FeSO4溶液难被氧化,请分析原因为________
(6)若产品质量为ag,则产率为________ %。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质的电离方程式如下:
HClO4=H++ClO4-;
Ba(OH)2=Ba2++2OH-;
Fe2(SO4)3=2Fe3++3SO42-;
KHSO4=K++H++SO42-
属于酸的物质是__________(写化学式);属于碱的物质是__________;属于盐的物质是______________。
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是________________________________。
②上述物质中既不是电解质也不是非电解质的是_________________
③写出纯碱的电离方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法标出下列反应中电子转移的方向和数目:_____________。
MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
此反应中,还原剂是 _______,氧化剂是 ________;_____元素被氧化,__元素被还原。由此可知,氧化还原反应的实质是__________________________________________。根据你的理解再写一个常见的氧化还原反应的化学方程式: _______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苄丙酮香豆素(H)常用于防治血觑栓栓塞性疾病。其合成路线如图所示(部分反应条件略去。)
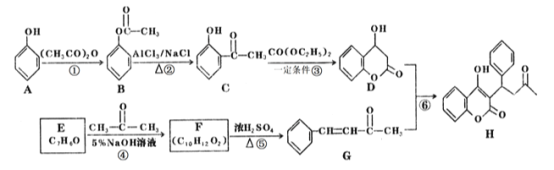
(1)E的名称是_________,D中含氧官能团的名称是_________。
(2)反应①的反应类型是__________,反应⑤的反应类型是_________。
(3)1mol H与H2加成,最多可消耗_____mol H2。
(4)反应③的化学方程式为____________________________________。
(5)C的同分异构体中满足下列条件的有______种,其中核磁共振氢谱有4组峰且峰面积之比为1:2:2:3的结构简式为__________(写一种即可)。
①不能和FeCl3溶液发生显色反应 ②1mol该有机物能与2molNaOH恰好完全反应
(6)参照苄丙酮香豆素的合成路线,设计一种以E和乙醛为原料制备![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.在共价化合物中一定含有共价键
B.含有共价键的化合物一定是共价化合物
C.含有离子键的化合物一定是离子化合物
D.全部由非金属组成的化合物可能是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙。反应的方程式如下:2Al+Fe2O3![]() 2Fe+Al2O3,下列说法不正确的是( )
2Fe+Al2O3,下列说法不正确的是( )
A. 氧化剂是Fe2O3,氧化产物是 Al2O3。
B. 被氧化的元素是铝,被还原的元素是铁。
C. 当转移的电子为0.3mol时,参加反应的铝为2.7g
D. Fe2O3既不是氧化剂又不是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com