
下列关于物质性质的叙述中,正确的是( )
A.Cl2能与金属活动顺序表中大多数金属反应
B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2
C.硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性
D.硅是应用广泛的半导体材料,常温下化学性质活泼
科目:高中化学 来源: 题型:
太阳能是清洁的新能源,为了环保,我们要减少使用像煤炭这样的常规能源而大力开发新能源。
(1)划分下列能源的类别。
煤、石油、水力、汽油、铀、薪柴、酒精、天然气、液化气、热水、煤气、蒸汽、风力、电
| 类别 | 一次能源 | 二次能源 |
| 燃料能源 | ||
| 非燃料能源 |
(2)煤、石油、天然气和生物质能作为能源的共同特点是______________,能量形成和转换利用过程基本上是________。
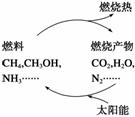
(3)为了消除大气污染,节约燃料,缓解能源危机,化学家提出了利用太阳能促使燃料循环使用的构想图,该设想的物质循环中太阳能最终转化为________,主要需解决的问题是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学式为C2H6O的化合物A具有如下性质:A+Na―→慢慢产生气泡
A+CH3COOH 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是
( )。
A.一定含有—OH B.一定含有—COOH
C.A为乙醇 D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作______。
(3)A与钠反应的化学方程式:_____________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
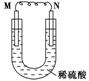
如图所示的装置中,M为金属活动性顺序表中位于氢之前的金属,N为石墨棒,下列关于此装置的叙述中不正确的是
( )。
A.N上有气体放出
B.M为负极,N为正极
C.是化学能转变为电能的装置
D.导线中有电流通过,电流方向是由M到N
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应______________________________________
银片上发生的电极反应______________________________________
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
①产生氢气的体积(标准状况);②通过导线的电量。(已知NA=6.02×1023 mol-1,电子电荷为1.60×10-19 C)
查看答案和解析>>
科目:高中化学 来源: 题型:
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题。
Ⅰ.探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
(1)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸 ②稀硫酸 ③浓硝酸 ④稀硝酸,能随即发生反应的是(填序号,下同)____________,微热则发生反应的是____________,加热后发生反应的是__________,加热也不发生反应的是____________。由此可以得到上述四种酸氧化性由强到弱的顺序是__________________________________。
(2)
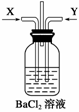
先将铜与浓硫酸反应产生的气体X持续通入如右图所示装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括________(选填序号)。
A.通入X气体后产生白色沉淀 B.通入X气体后溶液中无明显现象
C.通入Y气体开始产生沉淀 D.通入Y气体后沉淀溶解
E.通入Y气体后溶液中无明显现象
(3)由此可得到的结论是________(选填序号)。
A.HNO3的酸性比H2SO4强 B.盐酸的酸性比H2SO3强
C.BaSO3能溶于盐酸 D.HNO3能氧化H2SO3(或SO2)
E.BaSO4不溶于水也不溶于HNO3溶液
Ⅱ.下图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请回答下列问题:
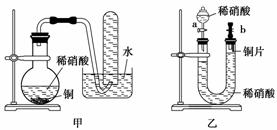
(1)写出铜和稀硝酸反应的离子方程式:_____________________________________。
(2)实验装置甲能否证明铜和稀硝酸反应的产物是NO气体________(填“能”或“不能”),请简述理由(用文字和化学方程式表示):__________________________________
________________________________________________________________________。
(3)若用实验装置乙进行实验,检查装置气密性的操作是_______________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.12 g铁粉加入25 mL 2 mol/L的FeCl3溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B.往溶液中滴入无色KSCN溶液,不显红色
C.Fe2+和Fe3+物质的量之比为6∶1
D.氧化产物和还原产物的物质的量之比为2∶5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com