
【题目】芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸 。反应原理:
![]() +2KMnO4
+2KMnO4 ![]() +KOH+2MnO2 +H2O
+KOH+2MnO2 +H2O
![]() +HCl
+HCl![]() +KCl
+KCl
反应试剂、产物的物理常数:
名称 | 相对分 子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
水 | 乙醇 | 乙醚 | ||||||
甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
主要实验装置和流程如下:
下图回流搅拌装置
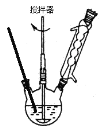
下图抽滤装置

实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
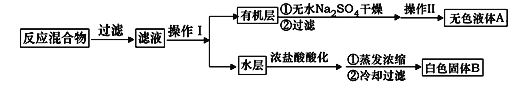
(1)无色液体A的结构简式为___________。操作Ⅱ为__________。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是______。
(3)下列关于仪器的组装或者使用正确的是__________。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入__________,分液,水层再加入__________,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100ml溶液,取其中25.00ml溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为______________。
【答案】(1)![]() (2分) 蒸馏(2分)
(2分) 蒸馏(2分)
(2)除去未反应的高锰酸钾氧化剂,否则用盐酸酸化时会发生盐酸被高锰酸钾所氧化,产生氯气;(2分)
(3)ABD (2分)漏选得一分,错选不得分
(4) NaOH溶液(2分) 浓盐酸酸化(2分) (5) 96% (2分)
【解析】
试题(1)结合操作目的,分析流程知:对反应后的溶液过滤除去生成的MnO2,滤液经分液所得有机层含有末反应的甲苯,水层含有生成的苯甲酸钾及其它可溶性物质。有机层经干燥剂干燥、过滤后,再经操作II得到的无色液体A应为甲苯。操作II为蒸馏。(2) 滤液呈紫色,证明高锰酸钾有剩余,又因为高锰酸钾会与浓盐酸反应产生氯气,所以应先加KHSO4除去末反应的高锰酸钾,再加浓盐酸酸化。(3) A、抽滤可以加快过滤速度,得到较干燥的沉淀;故A正确。
B、安装电动搅拌器时,搅拌棒下端不能与三颈烧瓶底、温度计等接触;故B正确。C、三颈烧瓶不能直接加热;故C不正确。D冷凝管中水的流向应是下进上出。故D正确。(4) 除去残留在苯甲酸中的甲苯时,先加入NaOH溶液,使苯甲酸转化为可溶性的苯甲酸钠溶于水,再经分液操作,将甲苯(有机层)除去,然后用浓盐酸把可溶性的苯甲酸钠转化为苯甲酸。(5) 根据关系式:
![]() --KOH
--KOH
122g 1mol
m 4×2.4×10-3mol
m=122g×4×2.4×10-3mol /1mol= 1.1712g
产品中苯甲酸质量分数为:1.1712g/1.22g×100%=96%


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图1所示。
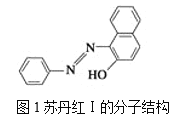
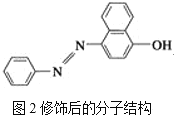
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会____(填“增大”或“减小”),原因是__________________。
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的结构式为__________,第二种配合物的结构式为_____。
(3)Ag+能与NH3、S2O32-、CN等形成配位数为2的配合物。
利用AgNO3和氨水可配制[Ag(NH3)2]OH溶液,在[Ag(NH3)2]OH中存在的化学键的类型有_____(填字母)。
A 离子键 B 金属键 C 配位键 D 非极性键 E 极性键
(4)NO3-中N原子的杂化轨道类型是____,空间构型为_____。写出一种与NO2-,SO2互为等电子体的短周期元素单质分子的化学式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机物,其中A是化学实验中常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图甲所示:
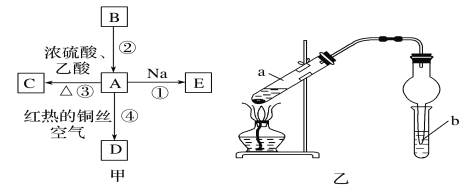
(1)C的结构简式__;A中官能团的名称为__。
(2)写出下列反应的化学方程式:
反应①__;
反应④__。
(3)实验室利用反应③制取C,常用图乙装置:
①a试管中主要反应的化学方程式为__。反应类型是__。
②在实验中用到了:铁架台(铁夹),酒精灯,试管,导管(橡胶管)和__。(填仪器名称)
③试管b中溶液名称为__,实验后观察到的现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5 mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应
根据上述信息,对X的结构判断正确的是 ( )
A.X中肯定有碳碳双键
B.X中可能有三个羟基和一个-COOR官能团
C.X中可能有三个羧基
D.X中可能有两个羧基和一个羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氧化性:Cl2 > Fe3+ >SO2,某化学研究性学习小组用图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕):
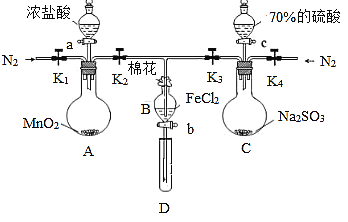
Ⅰ.打开弹簧夹K1—K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1,K3,K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
回答下列问题:
(1)过程Ⅰ的目的是________。
(2)棉花中浸润的溶液为________,作用是_____________。
(3)导致步骤Ⅲ中溶液变黄的离子反应是____,用_____,(写试剂化学式)检验氧化产物,现象是____。
(4)能说明氧化性Fe3+>SO2的离子方程式是________。
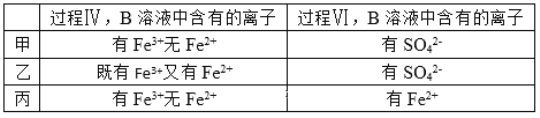
(5)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2> Fe3+>SO2的是__(填“甲”“乙”“丙”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C3H6)是基本有机化工原料。由A制备聚合物C和![]() 的合成路线(部分反应条件略去)如图所示:
的合成路线(部分反应条件略去)如图所示:
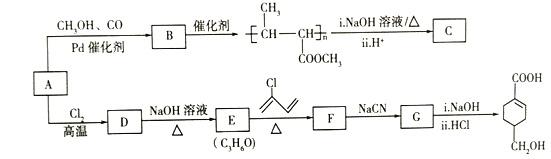
已知: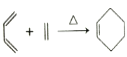 ;
;![]() +R-COOH
+R-COOH
回答下列问题:
(1)A的名称是_______,B中含氧官能团的名称是_______________。
(2)C的结构简式为_______________,D→E的反应类型为________________。
(3)E→F的化学方程式为____________________________。
(4)![]() 发生缩聚反应生成有机物的结构简式为_________________。
发生缩聚反应生成有机物的结构简式为_________________。
(5)B的同分异构体中,与B具有相同的官能团且能发生银镜反应的共有________种;其中核磁共振氢谱为3组峰,且峰面积之比为6:1:1的是________________(写结构简式)。
(6)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选)。_________________。合成路线流程图示例如下:A![]() B……
B……![]() 目标产物。
目标产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活和健康。因此采取改善能源结构、机动车限号等措施来减少PM2.5、SO2、NOx等污染。请回答下列问题:
Ⅰ. 臭氧是理想的烟气脱硝剂,其脱硝的反应之一为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
N2O5(g)+O2(g),不同温度下,在两个恒容容器中发生该反应,相关信息如下表及图所示,回答下列问题:
容器 | 甲 | 乙 |
容积/L | 1 | 1 |
温度/K | T1 | T2 |
起始充入量 | 1molO3和2molNO2 | 1molO3和2molNO2 |
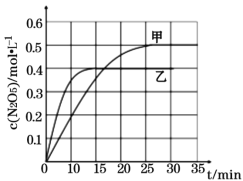
①0~15min内乙容器中反应的平均速率:v(NO2) =____(计算结果保留两位小数)。
②该反应的正反应为____(填“吸热”或“放热”)反应。
③T1时平衡后,向恒容容器中再充入1molO3和2molNO2,再次平衡后,NO2的百分含量将____(填“增大”“减小”或“不变”)。
④反应体系在温度为T1时的平衡常数为____。
⑤在恒温恒容条件下,下列条件不能证明该反应已经达到平衡的是____。
a.容器内混合气体压强不再改变
b.消耗2n molNO2的同时,消耗了n molO3
c.混合气体的平均相对分子质量不再改变
d.混合气体密度不再改变
II. 某化学小组查阅资料后得知:2NO(g)+O2(g) ![]() 2NO2(g) 的反应历程分两步:
2NO2(g) 的反应历程分两步:
①2NO(g)=N2O2(g) (快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
②N2O2(g)+O2(g)=2NO2(g) (慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
请回答下列问题:
(1)已知决定2NO(g)+O2(g) ![]() 2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
(2)一定温度下,反应2NO(g)+O2(g) ![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用金属钠还原CCl4和SiCl4制得一种一维SiC纳米棒。相关反应的化学方程式为8Na+CCl4+SiCl4![]() SiC+8NaCl。下列说法不正确的是
SiC+8NaCl。下列说法不正确的是
A. 一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力
B. 上述反应中SiC既是氧化产物又是还原产物
C. SiCl4是由极性键构成的非极性分子
D. 每生成1 mol SiC转移8 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、HCO3-、S2-、SO42-、Cl-、OH-中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如下:
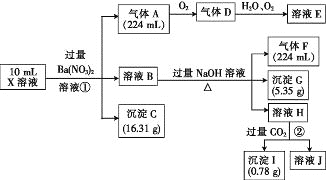
(1)通过上述实验过程,一定不存在的离子是_______。
(2)反应①中生成A的离子方程式为________。
(3)若测得X溶液中c(H+)=6mol·L-1,则X溶液中_______(填“含”或“不含”)Fe3+,c(Fe3+)=________mol·L-1(若填不含,则不需计算),X溶液中c(Cl-)=_______mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com