
(1)配平该反应并标出电子转移的方向和数目:KMnO4+HCl = MnCl2+ KCl+ Cl2↑+ H2O
(2)氧化剂是________________,氧化产物是__________________ (填化学式)。
(3)若生成71 g Cl2消耗的HCl是___________________,被氧化的HCl是_______________。
(4)CS2(液体)能在O2中完全燃烧,生成CO2和SO2,若将0.1 mol CS2在1 mol O2中完全燃烧,所得混合气体在标准状况下所占的体积为__________L。
Ⅱ、(6分)(1)下列A. B. C. D 是中学常见的混合物分离或提纯的基本装置
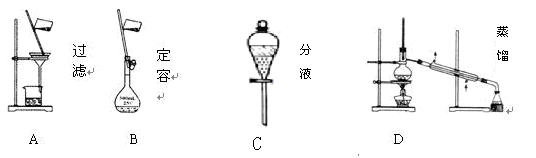
请根据实验需要将A. B.C. D装置填入适当的空格中。
①分离汽油和氯化钠溶液____________________
②用自来水制取蒸馏水__________________
③除去粗盐溶液中悬浮的泥沙_______________________________
(2)检验Fe3+常用的试剂除碱外,还可以将KSCN溶液滴入待检测溶液中,其产生的现象是______
________________________,发生反应的离子方程式________________________________。
(1)2KMnO4+16HCl =2MnCl2+2KCl+5Cl2↑+8H2O(4分,单双线桥均可)
(2)KMnO4,Cl2(每空1分,填化学式才给分)
(3)3.2 mol,2 mol。(每空1分,不带单位不给分)
(4)22.4 (2分)
Ⅱ.(6分)
(1)① C(1分) ② D(1分) ③A (1分)
(2)溶液变为血红色,(1分) Fe3+ + 3SCN- = Fe (SCN)3 (2分)
【解析】
试题分析:Ⅰ(1)锰由正7价还原为正2价,氯由负1价氧化为0价。
(2)氧化剂得到电子被还原,还原剂失去电子被氧化。
(3)71g氯气是1mol,根据化学方程式可知,消耗的氯气是3.2 mol,被氧化的氯气是2 mol。
(4)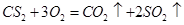 ,反应前后气体的体积不变。
,反应前后气体的体积不变。
Ⅱ(1)①汽油和氯化钠不相容用分液;②蒸馏使水先变成蒸汽再冷凝成水,除去杂质;③过滤是指在推动力或者其他外力作用下悬浮液(或含固体颗粒发热气体)中的液体(或气体)透过介质,固体颗粒及其他物质被过滤介质截留,从而使固体及其他物质与液体(或气体)分离的操作;
(2)生成了络合物。
考点:氧化还原反应和试验操作。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届上海理工大学附属中学高二上学期选修摸底考试化学试卷 题型:填空题
(9分)某一反应体系中有反应物和生成物共6种:HC1、H2SO4、SnC12、SnC14、FeSO4、Fe2(SO4)3,反应前在溶液中滴加KSCN溶液显红色,反应后红色消失。
(1)该反应的氧化剂是 。
(2)在该反应中,发生氧化反应的过程是 → 。
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目: 。
(4)SnC14与SnC12可用Hg2+来鉴别,HgC12与SnC12反应的产物是SnC14和Hg2C12(白色沉淀),该反应中还原剂与氧化剂的物质的量之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com