
| A、将AlCl3溶液加热蒸干可得AlCl3固体 |
| B、实验室配制氯化铁溶液时通常需要加入盐酸,目的是抑制铁离子水解 |
| C、将AlCl3溶液和Na2S溶液混合可得到Al2S3沉淀 |
| D、向氯化铵溶液中加入少量的硫酸铁固体,浓度会减少 |


科目:高中化学 来源: 题型:
 在如图所示的物质转化关系中,A是常见的碱性气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是排在金属活动性顺序氢后的紫红色金属单质.(部分反应中生成物没有全部列出,反应条件未列出)请回答下列问题:
在如图所示的物质转化关系中,A是常见的碱性气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是排在金属活动性顺序氢后的紫红色金属单质.(部分反应中生成物没有全部列出,反应条件未列出)请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
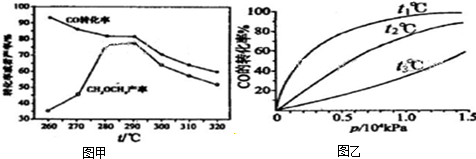
查看答案和解析>>
科目:高中化学 来源: 题型:
 图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu,b极:Fe-2e一=Fe2+,下列说法中不正确的是( )
图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu,b极:Fe-2e一=Fe2+,下列说法中不正确的是( )| A、该装置可能是电解池 |
| B、a极上发生的是还原反应 |
| C、a、b不可能是同种电极材料 |
| D、该装置工作时,溶液中的阴离子向b极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NH
| ||||||
| B、Ag+、Na+、[Al(OH)2]+、Cl- | ||||||
C、K+、NH
| ||||||
D、K+、Na+、NO3-、HCO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置.则下列说法正确的是( )
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置.则下列说法正确的是( )| A、甲装置中锌为负极,发生还原反应 |
| B、甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C、乙装置中铁极为阳极,电极反应式为:2Na++2e-═2Na |
| D、乙装置中B是氯气出口,A是钠出口 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0.1mol?L-1 NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| B、25℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
| C、在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 |
| D、将氨水和盐酸混合后,所得溶液中可能存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、483.6 kJ |
| B、88 kJ |
| C、285.8 kJ |
| D、44 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com