
| A£®¢Ł¢Ś¢Ū | B£®¢Ū¢Ł¢Ś | C£®¢Ś¢Ł¢Ū | D£®¢Ū¢Ś¢Ł |


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®PCl5ÖŠĖłÓŠµÄŌ×Ó¶¼Āś×ć×īĶā²ć8µē×Ó½į¹¹ |
| B£®Ķ¬ĖŲŅģŠĪĢåÖ®¼äµÄ×Ŗ»ÆŹōÓŚĪļĄķ±ä»Æ |
| C£®ÖŹ×ÓŹżĻąµČ£¬µē×ÓŹżŅ²ĻąµČµÄĮ¼ÖÖĪ¢Į£æÉÄÜŹĒ²»Ķ¬µÄĄė×Ó |
| D£®CaF2ŗĶNa2O2µÄ»Æѧ¼üŗĶ¾§ĢåĄąŠĶ¾łĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
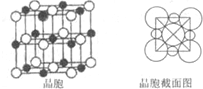
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
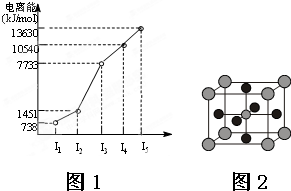
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŅŅ“¼ÕōĘūĶعż×ĘČȵÄCuO·ŪÄ© | B£®¶žŃõ»ÆĢ¼ĶعżNa2O2·ŪÄ© |
| C£®ĀĮÓėFe2O3·¢ÉśĀĮČČ·“Ó¦ | D£®½«ŠæĮ£Ķ¶ČėCu(NO3)2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®»īŠŌĢ攢SO2”¢ĀČĖ®¶¼»įŅņ·¢ÉśŃõ»Æ»¹Ō·“Ó¦¶ųŹ¹Ę·ŗģČÜŅŗĶŹÉ« |
| B£®Na2O2”¢H2O2Ėłŗ¬»Æѧ¼üĶźČ«ĻąĶ¬£¬¶¼ÄÜ×÷¹©Ńõ¼Į |
| C£®³£ĪĀĻĀ£¬ÅØĮņĖį”¢ÅØĻõĖįÓėĀĮ¾łÄÜ·¢Éś¶Ū»Æ£¬¾łÄÜÓĆĀĮ¹Ž“¢ŌĖ |
| D£®Ė®²£Į§£¬“Ó·ÖĄą·ØµÄ½Ē¶Č£¬æÉæ“×÷“æ¾»Īļ£¬æÉÓĆÓŚÄ¾²ÄµČµÄ·Ą»š¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĻņĢś·ŪÖŠ¼ÓČėĻ”ĻõĖį |
| B£®ĻņÉÕ¼īČÜŅŗÖŠĶØČėCO2ĘųĢå |
| C£®ĻņĻ”ŃĪĖįÖŠµĪČėÉŁĮæµÄNaAlO2ČÜŅŗ |
| D£®ĻņMgSO4”¢H2SO4µÄ»ģŗĻČÜŅŗÖŠ¼ÓČė¹żĮæµÄBa(OH)2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com