
ΓΨΧβΡΩΓΩΙηΓΔΝΉΓΔΝρΓΔ¬»ΕΦ «ΒΎ»ΐ÷ήΤΎΒΡΖ«Ϋπ τ‘ΣΥΊΘ§ΥϋΟ«‘ΎΙΛ≈©“Β…ζ≤ζ÷–ΕΦ”–÷Ί“ΣΒΡ”ΟΆΨΓΘ
Θ®1Θ© ΜυΧ§Ιη‘≠Ή”ΒΡΒγΉ”≈≈≤ΦΆΦΈΣ_________________________________________________ΘΜΝρΒΡΜυΧ§‘≠Ή”ΡήΝΩΉνΗΏΒΡΒγΉ”‘Τ‘ΎΩ’Φδ”–________________Ηω…λ’ΙΖΫœρΘ§‘≠Ή”ΙλΒά≥ ________________–ΈΓΘ
Θ®2Θ©ΙηΓΔΝΉΓΔΝρΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ________________ΓΘ
Θ®3Θ©ΒΞ÷ ΝΉ”κCl2Ζ¥”ΠΘ§Ω…“‘…ζ≤ζPC13ΚΆPC15ΓΘΤδ÷–Ης‘≠Ή”Ψυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΒΡΜ·ΚœΈο÷–Θ§P‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣ________________Θ§ΤδΖ÷Ή”ΒΡΩ’ΦδΙΙ–ΆΈΣ________________ΓΘ
Θ®4Θ©H3PO4ΈΣ»ΐ‘Σ÷–«ΩΥαΘ§”κFe3+–Έ≥…H3[Fe(PO4)2]Θ§¥Υ–‘÷ ≥Θ”Ο”Ύ―Ύ±Έ»ή“Κ÷–ΒΡFe3+ΓΘΜυΧ§Fe3+ΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ__________ΘΜPO43-ΉςΈΣ___________ΈΣFe3+ΧαΙ©________________ΓΘ
Θ®5Θ©ΝΉΜ·≈πΘ®BPΘ© «“Μ÷÷≥§”≤ΡΆΡΞΆΩ≤ψ≤ΡΝœΘ§œ¬ΆΦΈΣΤδΨßΑϊΘ§≈π‘≠Ή””κΝΉ‘≠Ή”ΉνΫϋΒΡΨύάκΈΣa cmΓΘ ”ΟMg/mol±μ ΨΝΉΜ·≈πΒΡΡΠΕϊ÷ ΝΩΘ§NA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§‘ρΝΉΜ·≈πΨßΧεΒΡΟήΕ»ΈΣ_________g/cm3ΓΘ

ΓΨ¥πΑΗΓΩ ![]() 3 ―ΤΝε P>S>Si sp3‘”Μ· »ΐΫ«ΉΕ–Έ [Ar]3d5 ≈δΧε Ι¬ΒγΉ”Ε‘
3 ―ΤΝε P>S>Si sp3‘”Μ· »ΐΫ«ΉΕ–Έ [Ar]3d5 ≈δΧε Ι¬ΒγΉ”Ε‘ 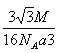
ΓΨΫβΈωΓΩΙηΓΔΝΉΓΔΝρΓΔ¬»ΕΦ «ΒΎ»ΐ÷ήΤΎΒΡΖ«Ϋπ τ‘ΣΥΊΘ§ΥϋΟ«‘ΎΙΛ≈©“Β…ζ≤ζ÷–ΕΦ”–÷Ί“ΣΒΡ”ΟΆΨΓΘ
Θ®1Θ© ΜυΧ§Ιη‘≠Ή”ΒΡΒγΉ”≈≈≤ΦΆΦΈΣ![]() ΘΜΝρΒΡΜυΧ§‘≠Ή”ΡήΝΩΉνΗΏΒΡΒγΉ”‘Τ «3pΙλΒάΘ§‘ΎΩ’Φδ”–3Ηω…λ’ΙΖΫœρΘ§‘≠Ή”ΙλΒά≥ ―ΤΝε–ΈΓΘ
ΘΜΝρΒΡΜυΧ§‘≠Ή”ΡήΝΩΉνΗΏΒΡΒγΉ”‘Τ «3pΙλΒάΘ§‘ΎΩ’Φδ”–3Ηω…λ’ΙΖΫœρΘ§‘≠Ή”ΙλΒά≥ ―ΤΝε–ΈΓΘ
Θ®2Θ©“ΜΑψΒΊΘ§Ζ«Ϋπ τ–‘‘Ϋ«ΩΒΡ‘ΣΥΊΘ§ΤδΒΎ“ΜΒγάκΡή‘ΫΗΏΓΘ”…”ΎΝΉΒΡ3pΙλΒά¥Π”ΎΫœΈ»Ε®Ακ≥δ¬ζΉ¥Χ§Θ§Υυ“‘ΤδΒΎ“ΜΒγάκΡήΗΏ”ΎΤδœύΝΎΒΡ‘ΣΥΊΓΘΙηΓΔΝΉΓΔΝρΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣP>S>Si ΓΘ
Θ®3Θ©ΒΞ÷ ΝΉ”κCl2Ζ¥”ΠΘ§Ω…“‘…ζ≤ζPC13ΚΆPC15ΓΘΤδ÷–PC13Ης‘≠Ή”Ψυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§Ζ÷Ή”÷–Φέ≤ψΒγΉ”Ε‘ ΐn=![]() =4Θ§P‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣsp3‘”Μ·Θ§ΤδΖ÷Ή”ΒΡΩ’ΦδΙΙ–ΆΈΣ»ΐΫ«ΉΕ–ΈΓΘ
=4Θ§P‘≠Ή”ΒΡ‘”Μ·ΙλΒάάύ–ΆΈΣsp3‘”Μ·Θ§ΤδΖ÷Ή”ΒΡΩ’ΦδΙΙ–ΆΈΣ»ΐΫ«ΉΕ–ΈΓΘ
Θ®4Θ©H3PO4ΈΣ»ΐ‘Σ÷–«ΩΥαΘ§”κFe3+–Έ≥…H3[Fe(PO4)2]Θ§¥Υ–‘÷ ≥Θ”Ο”Ύ―Ύ±Έ»ή“Κ÷–ΒΡFe3+ΓΘΜυΧ§Fe3+ΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ[Ar]3d5ΘΜPO43-ΉςΈΣ≈δΧεΈΣFe3+ΧαΙ©Ι¬ΒγΉ”Ε‘ΓΘ
Θ®5Θ©Α―ΗΟΨßΑϊΖ÷≥…8Ηω–ΓΝΔΖΫΧεΘ§Τδ÷–“ΜΗω–ΓΝΔΖΫΧεΒΡΕΞΒψΚΆΧε–Ρ÷°ΦδΒΡΨύάκΈΣ≈π‘≠Ή””κΝΉ‘≠Ή”ΉνΫϋΒΡΨύάκΘ§≈π‘≠Ή””κΝΉ‘≠Ή”ΉνΫϋΒΡΨύάκΈΣa cmΓΘ‘ΎΗΟΨßΑϊ÷–Θ§”–4ΗωB‘≠Ή”ΚΆ4ΗωP‘≠Ή”ΓΘ ”ΟMg/md±μ ΨΝΉΜ·≈πΒΡΡΠΕϊ÷ ΝΩΘ§NA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘ…ηΗΟΨßΑϊΒΡ±Ώ≥ΛΈΣ2xΘ§‘ρx2+2x2=(2a)2Θ§Ϋβ÷°ΒΟx=![]() aΘ§ΗΟΨßΑϊΒΡΧεΜΐΈΣΘ®2xΘ©3=
aΘ§ΗΟΨßΑϊΒΡΧεΜΐΈΣΘ®2xΘ©3=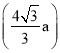 3ΓΘ1molΗΟΨßΑϊ÷–Κ§4molBPΘ§÷ ΝΩΈΣ4M gΘ§ΝΉΜ·≈πΨßΧεΒΡΟήΕ»ΈΣ=
3ΓΘ1molΗΟΨßΑϊ÷–Κ§4molBPΘ§÷ ΝΩΈΣ4M gΘ§ΝΉΜ·≈πΨßΧεΒΡΟήΕ»ΈΣ=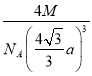 g/cm3=
g/cm3=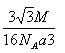 g/cm3ΓΘ
g/cm3ΓΘ


 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪ3.72g”…Ϋπ τΡΤΓΔ―θΜ·ΡΤΚΆΙΐ―θΜ·ΡΤΉι≥…ΒΡΜλΚœΈο”κΉψΝΩΥ°Ζ¥”ΠΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΟΒΫ672mLΜλΚœΤχΧεΘ°ΫΪΗΟΜλΚœΤχΧε”ΟΒγΜπΜ®Βψ»ΦΘ§«ΓΚΟΆξ»ΪΖ¥”ΠΘ§‘ρ‘≠ΜλΚœΈο÷–ΡΤΓΔ―θΜ·ΡΤΓΔΙΐ―θΜ·ΡΤΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣΘ® Θ©
A.3ΘΚ2ΘΚ1
B.4ΘΚ2ΘΚ1
C.2ΘΚ1ΘΚ1
D.1ΘΚ1ΘΚ1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “÷Τ»Γ¬»Τχ≥ΐΝΥ”Ο≈®―ΈΥαΚΆΕΰ―θΜ·ΟΧΖ¥”ΠΆβΜΙΩ…άϊ”Οœ¬Ν–Ζ¥”ΠΘΚKClO3+6HClΘ®≈®Θ©®TKCl+3Cl2Γϋ+3H2OΘ§ΗΟΖ¥”ΠΒΡ”≈Βψ «Ζ¥”Π≤ζ…欻ΤχΥΌΕ»ΩλΓΔ≤Μ–ηΦ”»»Θ°ΆΦ « Β―ι “άϊ”Ο¥ΥΖ¥”Π÷Τ±Η¬»Τχ≤ΔΫχ––“ΜœΒΝ–œύΙΊ Β―ιΒΡΉΑ÷ΟΘ®Φ–≥÷…η±Η“―¬‘Θ©Θ° 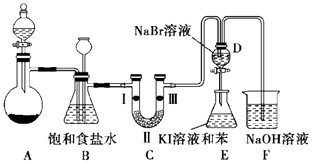
Θ®1Θ©…œ ωΖ¥”Π÷– «―θΜ·ΦΝΘ§ «ΜΙ‘≠ΦΝΘ§»τΖ¥”Π÷–―θΜ·≤ζΈο±»ΜΙ‘≠≤ζΈοΕύ 1molΘ§‘ρΉΣ“ΤΒΡΒγΉ” ΐΡΩΈΣ Θ°
Θ®2Θ©ΉΑ÷ΟBΒΡΉς”Ο « Θ§ Β―ιΫχ–– ±C÷–Ω…ΡήΖΔ…ζΕ¬»ϊΘ§«κ–¥≥ωΖΔ…ζΕ¬»ϊ ±B÷–ΒΡœ÷œσΘΚ Θ°
Θ®3Θ©ΉΑ÷ΟCΒΡ Β―ιΡΩΒΡ «―ι÷Λ¬»Τχ «ΖώΨΏ”–Τ·ΑΉ–‘Θ§ΈΣ¥ΥC÷–ΔώΓΔΔρΓΔΔσ“ά¥ΈΖ≈»κΘ®―ΓΓΑaΓ±ΓΑbΓ±ΜρΓΑcΓ±Θ©
a | b | c | |
Δώ | Η…‘οΒΡ”–…Ϊ≤ΦΧθ | Σ»σΒΡ”–…Ϊ≤ΦΧθ | Σ»σΒΡ”–…Ϊ≤ΦΧθ |
Δρ | Φν ·Μ“ | ≈®ΝρΥα | ΈόΥ°¬»Μ·ΗΤ |
Δσ | Σ»σΒΡ”–…Ϊ≤ΦΧθ | Η…‘οΒΡ”–…Ϊ≤ΦΧθ | Η…‘οΒΡ”–…Ϊ≤ΦΧθ |
Θ®4Θ©…ηΦΤΉΑ÷ΟDΓΔE ΒΡΡΩΒΡ «ΈΣΝΥ±»ΫœCl2ΓΔBr2ΓΔI2ΒΡ―θΜ·–‘«Ω»θΘ° “―÷ΣBr2 ΒΡΥ°»ή“Κ“ρ≈®Ε»≤ΜΆ§Εχ≥ œ÷≥»…ΪΜρΚλΉΊ…ΪΘ§I2Ρ―»ή”ΎΥ°Εχ“Ή»ή±ΫΘ§«“ I2 ΒΡ±Ϋ»ή“ΚΈΣΉœΚλ…ΪΘ°Β±œρD÷–ΜΚΜΚΆ®»κΉψΝΩCl2 ±Θ§Ω…“‘Ω¥ΒΫΈό…Ϊ»ή“Κ÷πΫΞ±δΈΣΚλΉΊ…ΪΘ§ΥΒΟς Cl2ΒΡ―θΜ·–‘¥σ”Ύ Br2 Θ§ «κ–¥≥ωD÷–Ε‘”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ≤Δ”ΟΥΪœΏ«≈Ζ®±μ Ψ≥ωΒγΉ”ΉΣ“Τ«ιΩωΘΚ Θ° ¥ρΩΣΜν»ϊΘ§ΫΪ D÷–ΒΡ…ΌΝΩ»ή“ΚΦ”»κE÷–Θ§’ώΒ¥EΘ§Ιέ≤λΒΫE÷–»ή“ΚΖ÷ΈΣΝΫ≤ψΘ§…œ≤ψΘ®±Ϋ≤ψΘ©ΈΣΉœΚλ…ΪΘ°ΗΟœ÷œσΘ® ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©ΥΒΟςBr2ΒΡ―θΜ·–‘¥σ”ΎI2 Θ°
Θ®5Θ©ΉΑ÷ΟFΒΡΉς”Ο «≥ΐ»ΞΈέ»Ψ–‘ΒΡΈο÷ Θ®Cl2ΓΔBr2 Β»Θ©Θ§“―÷ΣCl2”κNaOHΖ¥”Π ±≤ζΈο÷–Ω…Ρή”–NaClΓΔNaClOΓΔNaClO3 Θ§ «“ ![]() ÷Β”κΈ¬Ε»ΗΏΒΆ”–ΙΊΘ° »τ…’±≠÷–ΉΑ”–500mL0.2mol/L ΒΡNaOH»ή“ΚΘ§‘ρΉνΕύΩ…Έϋ ’±ξΩωœ¬ΒΡCl2ΒΡΧεΜΐΈΣLΘ®Κω¬‘Cl2»ή”ΎΥ°Θ©Θ°
÷Β”κΈ¬Ε»ΗΏΒΆ”–ΙΊΘ° »τ…’±≠÷–ΉΑ”–500mL0.2mol/L ΒΡNaOH»ή“ΚΘ§‘ρΉνΕύΩ…Έϋ ’±ξΩωœ¬ΒΡCl2ΒΡΧεΜΐΈΣLΘ®Κω¬‘Cl2»ή”ΎΥ°Θ©Θ°
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25 Γφ ±Θ§œ¬Ν–ΥΡ÷÷»ή“Κ÷–Θ§”…Υ°Βγάκ…ζ≥…ΒΡ«βάκΉ”≈®Ε»÷°±» «Θ® Θ©
ΔΌ1 molΓΛLΘ≠1ΒΡ―ΈΥαΓΓ ΔΎ0.1 molΓΛLΘ≠1ΒΡ―ΈΥα
Δέ0.01 molΓΛLΘ≠1ΒΡNaOH»ή“ΚΓΓ Δή1 molΓΛLΘ≠1ΒΡNaOH»ή“Κ
A. 1ΓΟ10ΓΟ100ΓΟ1 B. 1ΓΟ10Θ≠1ΓΟ10Θ≠12ΓΟ10Θ≠14
C. 14ΓΟ13ΓΟ12ΓΟ14 D. 14ΓΟ13ΓΟ2ΓΟ1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊ”ΎΧ«άύΓΔ÷§ΖΨΚΆΒΑΑΉ÷ ΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. ΒμΖέΚΆœΥΈ§ΥΊΨυΩ…”Ο(C6H10O5)n±μ ΨΘ§“ρ¥ΥΥϋΟ«ΜΞΈΣΆ§Ζ÷“λΙΙΧε
B. ΤœΧ―Χ«Ω…“‘ΖΔ…ζ―θΜ·Ζ¥”ΠΚΆ“χΨΒΖ¥”ΠΘ§ΥΒΟςΤœΧ―Χ«ΨΏ”–ΜΙ‘≠–‘
C. Ά®Ιΐ―ΈΈω¥”»ή“Κ÷–Έω≥ωΒΡΒΑΑΉ÷ »‘Ρή»ήΫβ”ΎΥ°
D. ÷§ΖΨΡήΖΔ…ζ‘μΜ·Ζ¥”ΠΘ§…ζ≥…Η ”ΆΚΆΗΏΦΕ÷§ΖΨΥαΡΤ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩFe2O3+2Al ![]() Al2O3+2FeΥυ τΜυ±ΨΖ¥”Πάύ–Ά « Θ° ΗΟΖ¥”Π÷–Θ§Fe2O3ΖΔ…ζΝΥΖ¥”ΠΘ§ «―θΜ·ΦΝΘ§ «―θΜ·≤ζΈοΘ°
Al2O3+2FeΥυ τΜυ±ΨΖ¥”Πάύ–Ά « Θ° ΗΟΖ¥”Π÷–Θ§Fe2O3ΖΔ…ζΝΥΖ¥”ΠΘ§ «―θΜ·ΦΝΘ§ «―θΜ·≤ζΈοΘ°
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕΪ±±ΜΔ÷ς“ΣΖ÷≤Φ‘ΎΈ“Ιζ≥ΛΑΉ…ΫΓΔ–Γ–ΥΑ≤ΝκȼΘΜΜΣΡœΜΔ÷ς“ΣΖ÷≤Φ”ΎΈ“Ιζ≥ΛΫ≠Νς”ρ“‘ΡœΒΊ«χΓΘΗυΨίΈ“Ο«―ßΙΐΒΡ÷Σ Ε≈–ΕœΘ§ΕΪ±±ΜΔ”κΤδ…ζ¥φΜΖΨ≥œύ ”ΠΘ§”κΜΣΡœΜΔœύ±»Θ§œ¬Ν–ΡΡ÷÷Έο÷ Κ§ΝΩΥυ’Φ±»άΐΟςœ‘ΤΪΗΏ
A. Χ«‘≠ B. ÷§ΖΨ C. ΒΑΑΉ÷ D. ΚΥΥα
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ τ”Ύ”–ΜζΈο «(ΓΓΓΓ)
A. H2CO3 B. CaC2 C. C2H5Cl D. NH4HCO3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–»ή“Κ÷–Θ§»ή÷ ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ1molL©¹1ΒΡ «Θ® Θ©
A.ΫΪ40 g NaOH»ή”Ύ1 LΥ°ΥυΒΟΒΡ»ή“Κ
B.ΫΪ22.4 L HCl»ή”ΎΥ°≈δ≥…1 L»ή“Κ
C.1 LΚ§2 mol K+ΒΡK2SO4»ή“Κ
D.ΫΪ0.5 molL©¹1ΒΡNaNO3»ή“Κ100 mLΦ”»»’τΖΔΒτ50 g Υ°ΚσΒΡ»ή“Κ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com