2013年6月“蛟龙”号载人潜水器投入应用中,计划每年将有4至5个月的海上时间,可用于深海探矿.锰结核中的黄铜矿(CuFeS
2)是海洋矿物中的一种,它是制取铜及其化合物的主要原料之一,还可用于制备硫及铁的化合物.请回答下列问题:
(1)“蛟龙”号外壳用特殊的钛合金材料制成,它可以在深海中承受700个大气压的压力.下列说法正确的是
.
A.已知金属钛的原子序数为22,则其属于主族元素
B.钛合金强度很大
C.制备钛铝合金时可在空气中将两种金属混合后熔化而成
D.可用电解熔融二氧化钛的方法冶炼金属钛
(2)利用黄铜矿冶炼铜的反应为:8CuFeS
2+21O
2 8Cu+4FeO+2Fe
2O
3+16SO
2若CuFeS
2中Fe的化合价为+2,反应中被还原的元素是
(填元素符号),生成1mol Fe
2O
3转移电子的物质的量为
mol
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe
2O
3、FeO、SiO
2、Al
2O
3)可制备Fe
2O
3.方法如下:
a.用过量稀盐酸浸取炉渣,过滤.
b.滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe
2O
3.
①a中过滤的目的是
.
②除去Al
3+的化学方程式是
.
③b中将滤液氧化常选用H
2O
2,其反应的离子方程式为
.
④选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO
4溶液、NaOH溶液、碘水所选试剂为
. 证明炉渣中含有FeO的实验现象为
.
(4)将Cu放入0.1mol?L
-1 FeCl
3溶液中,反应一定时间后取出Cu片,溶液中c(Fe
3+):c(Fe
2+)=2:3,则Cu
2+与Fe
3+的物质的量之比为
.



 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案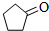 )可由环戊烷经三步反应合成:
)可由环戊烷经三步反应合成: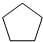
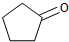

 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式为2CH4O+3O2=2CO2+4H2O,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式为2CH4O+3O2=2CO2+4H2O,如图是该燃料电池的示意图.下列说法错误的是( )