
| A. | H2O | B. | CaI2 | C. | KOH | D. | NaNO3 |
分析 金属元素和非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物.
解答 解:A.水分子中H-O原子之间只存在共价键,属于共价化合物,故A选;
B.碘化钙中钙离子和碘离子之间只存在离子键,属于离子化合物,故B不选;
C.KOH中钾离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,属于离子化合物,故C不选;
D.硝酸钠中钠离子和硝酸根离子之间存在离子键、N-O原子之间存在共价键,属于离子化合物,故D不选;
故选A.
点评 本题考查离子化合物和共价化合物的判断,侧重考查基本概念,根据物质构成微粒判断化合物类型,注意不能根据是否含有金属元素判断离子化合物,为易错题.


科目:高中化学 来源: 题型:选择题
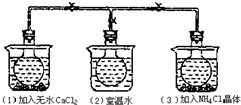 如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )
如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中.在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是( )| A. | CaCl2溶于水时放出热量 | B. | 烧瓶(1)中气体的压强增大 | ||
| C. | NH4Cl溶于水时放出热量 | D. | 烧瓶(3)中气体的压强减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
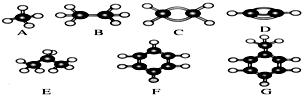
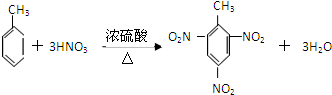 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过分馏可得到焦炉气、煤焦油和焦炭 | |
| B. | 甲烷、汽油、酒精都是碳氢化合物,都可作燃料 | |
| C. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| D. | 蛋白质、淀粉、油脂均能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
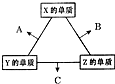 X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16.在适当条件下三种单质两两化合,可发生如图所示变化.己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个.请回答下列问题:由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为HNO3、NH4NO3、NH3.H2O.
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16.在适当条件下三种单质两两化合,可发生如图所示变化.己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个.请回答下列问题:由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为HNO3、NH4NO3、NH3.H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水 | B. | 干冰受热直接变成气体 | ||
| C. | HCl溶解于水 | D. | 打雷放电时,O2变成O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com