
����Ŀ������ƹ㷺����ʳƷ��������ʯ�͵ȹ�ҵ�����ϣ�300��400�����ҷֽ⣮ 
��1��ʵ������ȡ�ķ���֮һ�ǣ�Ca��OH��2+2HCHO+H2O2=Ca��HCOO��2+2H2O+H2����
ʵ������ȡʱ������ҵ���������ƺͼ�ȩ���μ��뵽��������Ϊ30��70%�Ĺ���������Һ�У�Ͷ�����ʵ���֮������Ϊ1��2��1.2�������տɵõ���������98%�������ؽ����������͵����ʲ�Ʒ��
��I��������������������Զ࣬��Ŀ���� ��
��II����Ӧ�¶���ÿ�����30��70��֮�䣬�¶Ȳ����ߣ�����Ҫԭ���� ��
��III���Ʊ�ʱ�ڻ����Һ��Ҫ���������������Ƽ�ȩ��������Ӧ�⣬��Ҫ����������Na2S��Һ�������Ƶ�Ŀ���� ��
��IV��ʵ��ʱ��ǿ������45min����Ŀ�������������������Һ��pH 7��8����Ŀ���� �� ��ᾧ���롢����ò�Ʒ��
��2��ij�о���ѧϰС���ù�ҵ̼��ƣ���Ҫ�ɷ�ΪCaCO3������Ϊ��Al2O3��FeCO3�� Ϊԭ�ϣ����Ʊ������Σ������������Һ�����ȡ����ƣ������ͼ�������ʵ��ܽ������������ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0molL��1���㣩�����ṩ���Լ��У�a�������ƣ�b.5molL��1���ᣬc.5molL��1���ᣬd.5molL��1���ᣬe.3%H2O2��Һ��f������ʯ��ˮ��
���� | ��ʼ���� | ������ȫ |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
ʵ�鲽��
����1����ȡ13.6g����������Լ20mLˮ�������Һ���ã�����ȡ��ϸ��̼�����Ʒ10g���ã�
����2�� ��
����3�� ��
����4�����˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������Ũ������ϴ�ӡ�60��ʱ����ü���ƾ��壮
���𰸡�
��1��ʹ��ȩ������������ȩ�������ʺͲ�Ʒ���ȣ���ֹH2O2�ֽ�ͼ�ȩ�ӷ�����ȥ�ؽ������ӣ�ʹ��Ӧ���ֽӴ�����߲��ʣ���ֹ�����ˮ��
��2�����Թ��������ܽ�̼�����Ʒ����ʯ��ˮ������ҺpH=5�����ȹ���
���������⣺��1����I����ѧ��Ӧ��һ�ַ�Ӧ�����Ŀ���Ǵٽ�������Ӧ���ַ�Ӧ�����ת���ʣ���ӹ����Ĺ���������ʹ��ȩ������������ȩ�������ʺͲ�Ʒ���ȣ����Դ��ǣ�ʹ��ȩ������������ȩ�������ʺͲ�Ʒ���ȣ���II���¶Ƚϸ�ʱ��˫��ˮ�ֽ⣬��ȩ�ӷ�����Ӧ�¶���ÿ�����30��70��֮�䣬�¶Ȳ����ߣ��ܷ�ֹH2O2�ֽ�ͼ�ȩ�ӷ���
���Դ��ǣ���ֹH2O2�ֽ�ͼ�ȩ�ӷ�����III���Ʊ�ʱ�ڻ����Һ��Ҫ���������������Ƽ�ȩ��������Ӧ�⣬��Ҫ����������Na2S��Һ���������ؽ������ӽ�������������������ˮ�����Գ�ȥ�ؽ������ӣ�
���Դ��ǣ���ȥ�ؽ������ӣ���IV��������ʹʹ��Ӧ���ֽӴ���ʹ�䷴Ӧ��ȫ����߲��ʣ����������Ϊ��������ӣ�������ˮ���������ԣ�������ҺpH 7��8����ҺΪ�����������Ƽ����ˮ�⣬���Դ��ǣ�ʹ��Ӧ���ֽӴ�����߲��ʣ���ֹ�����ˮ�⣻��2����ʵ������Ҫȥ�����ʣ�ͬʱ���ɿ����Ը��Σ�������������������Ҫ����Ϊ�����ӣ�˫��ˮ�����ᣩ������������������ȥ��������ҲҪ���ɼ��ȥ���ʵ���pHΪ5����ʯ��ˮ���ڣ���Ȼ������������Һ��������ܽ�Ƚ�С�����¶ȱ仯�������Ǽ���ƣ�������Ũ�����õ�����ƹ��壬���ȹ��ˣ���ֹ��������������
�����IJ�����
����1����ȡ13.6g����������Լ20mLˮ�������Һ���ã�����ȡ��ϸ��̼�����Ʒ10g���ã�
����2�����Թ��������ܽ�̼�����Ʒ��
����3����ʯ��ˮ������ҺpH=5��
����4�����˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������Ũ�������ȹ��ˡ�ϴ�ӡ�60��ʱ����ü���ƾ��壬
���Դ��ǣ����Թ��������ܽ�̼�����Ʒ����ʯ��ˮ������ҺpH=5�����ȹ��ˣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ����( )
A. �ڹ��ۻ�������Ҳ���ܺ������Ӽ�
B. �ǽ���֮���γɵĻ�ѧ����һ���ǹ��ۼ�
C. ���й��ۼ��Ļ����ﲻһ���ǹ��ۻ�����
D. �������Ӽ��Ļ�����һ�������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������B3N3H6�������뱽�ķ��ӽṹ���ƣ���ͼ��ʾ������������ȡ���B3N3H2Cl4����ͬ���칹�����ĿΪ�� �� 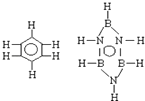
A.2
B.3
C.4
D.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A��1 mol H2O������Ϊ18g/mol
B��CH4��Ħ������Ϊ16g
C��3.01��1023��SO2���ӵ�����Ϊ32g
D����״������1 mol�κ����������Ϊ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�ؿ��γ��⻯�±����������������������ȶ��ֻ����
��1���£�N2H4�����������ȼ�ϣ���ԭ���ǣ�N2O4��l��+2N2H4��l��=3N2��g��+4H2O��g��������Ӧ����4mol N��H�����ѣ����γɵĦм���mol��N2H4�ķе��C2H6����Ҫԭ���� ��
��2��F2����NH3��ͭ�������·�Ӧ����NF3 �� NF3���ӵĿռ乹��Ϊ ��
��3�����Ͱ�����640��ɷ����û���Ӧ������֮һ�ľ����ṹ��ͼ��д���÷�Ӧ�Ļ�ѧ����ʽ�� �� 
��4���������ƣ�NaN3���ֽⷴӦΪ��2NaN3��s��=2Na��l��+3N2��g���������й�˵����ȷ����������ţ���
a�������£�N2���ȶ�������ΪN�ĵ����ܴ�
b���ƾ����ṹ��ͼ2��ÿ����������5����ԭ��
c����һ�����ܣ�I1����N��O��P��S
d��NaN3��KN3�ṹ���ƣ������ܣ�NaN3��KN3
��5�������Y�Ľṹ��ͼ3��Y�к���������ţ���
a�����Թ��ۼ� b���Ǽ��Թ��ۼ� c����λ�� d�����
Y��̼ԭ�ӵ��ӻ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ����˵����ȷ���� (�� ��)
A. �л�ѧ�����ѵı仯һ���ǻ�ѧ�仯
B. CaCl2�����к������Ӽ��ͷǼ��Լ�
C. ���ۻ�������һ��ֻ���й��ۼ�
D. ֻ���ǽ���Ԫ�ص�����һ���������Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱽ������ ![]() ���㷺�����ڿɿɡ����ȡ���ݮ�������У�������ʳ����ջ���Ʒ���㾫����֪��X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����ҵ�Ͽ���X�ͼױ��˹��ϳ����ᱽ��������ϳ�·�����£�
���㷺�����ڿɿɡ����ȡ���ݮ�������У�������ʳ����ջ���Ʒ���㾫����֪��X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����ҵ�Ͽ���X�ͼױ��˹��ϳ����ᱽ��������ϳ�·�����£� 
�ݴ˻ش��������⣺
��1����Ӧ����Y����A�Ļ�ѧ����ʽΪ ������A�к��й����ŵ�����Ϊ ��
��2��ʵ����Ϊ����A��B���ߵ�ˮ��Һ������ѡ�õĻ�ѧ�Լ��� �� A��������Һ B��NaOH��Һ C�������� D��������Һ
��3����д����Ӧ�ݵĻ�ѧ����ʽ ��
��4��д�������������������ᱽ������һ��ͬ���칹�壺 �ٺ������ṹ���ھ������Ľṹ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ��Դ�Ŀ������ù���ֻ�漰�����仯����
A. ��¯����B. ��ˮɹ��C. ˮ�ĵ��D. ��ʳ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com