
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
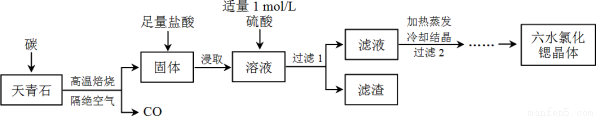
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是_________________________________________。
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_____________________________________________。
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_______________。
(4)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(5)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(1)天青石焙烧前先研磨粉碎,其目的是为了增加反应物的接触面积,提高化学反应速率。
(2)SrSO4 + 4C 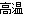 SrS + 4CO↑
SrS + 4CO↑
(3)洗涤、干燥(或烘干)
(4)除去溶液中Ba2+杂质 0.03
(5)溶液由无色变为血红色,且30 s不褪色 93.45%
【解析】
试题分析:(1)天青石焙烧前先研磨粉碎,其目的是为了增加反应物的接触面积,提高化学反应速率,从而提高原料的转化率。(2)在焙烧的过程中若只有0.5 mol SrSO4中只有S被还原,转移了4 mol电子,则1mol的S转移8mol的电子,由于在反应前元素的化合价为+6价,所以反应后元素的化合价为-2价。因此碳与天青石在高温下发生反应SrSO4 + 4C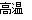 SrS + 4CO↑,(3)然后向得到的含有SrS固体中加入HCl发生反应:SrS+2HCl= SrCl2+H2S↑,将溶液蒸发浓缩、冷却结晶,然后从溶液中将晶体过滤出来,洗涤除去表面的杂质离子并进行干燥即SrCl2·6H2O。(4)在用HCl溶解SrS后的溶液中加入硫酸的目的是除去溶液中Ba2+杂质。由于在Ba2+浓度为1×10-5 mol/L,BaSO4的溶度积常数为1.1×10-10;所以c(SO42-)=1.1×10-10÷1×10-5=1.1×10-5mol/L。而SrSO4的溶度积常数为3.3×10-7,所以c(Sr2+)=3.3×10-7÷1.1×10-5=3.0×10-2=0.03mol/L。(5)若NH4SCN不再剩余的Ag+ 结合形成AgSCN白色沉淀,溶液中就会含有SCN-,就会与Fe3+产生络合物是溶液变为红色。因此滴定达到终点时溶液由无色变为血红色,且30 s不褪色。n(NH4SCN)=0.2000 mol/L×0.02L=4.0×10-3mol,所以溶液中剩余的Ag+的物质的量为n(Ag+)=4.0×10-3mol,因此与Cl―反应的Ag+的物质的量为n(Ag+)=1.100×10-2 mol -4.0×10-3mol=7.0×10-3mol n(SrCl2·6H2O)=3.5×10-3mol,m(SrCl2·6H2O)= 3.5×10-3mol×267 g/mol=0. 9345g. 所以产品纯度为0. 9345g÷1g×100%=93.45%.
SrS + 4CO↑,(3)然后向得到的含有SrS固体中加入HCl发生反应:SrS+2HCl= SrCl2+H2S↑,将溶液蒸发浓缩、冷却结晶,然后从溶液中将晶体过滤出来,洗涤除去表面的杂质离子并进行干燥即SrCl2·6H2O。(4)在用HCl溶解SrS后的溶液中加入硫酸的目的是除去溶液中Ba2+杂质。由于在Ba2+浓度为1×10-5 mol/L,BaSO4的溶度积常数为1.1×10-10;所以c(SO42-)=1.1×10-10÷1×10-5=1.1×10-5mol/L。而SrSO4的溶度积常数为3.3×10-7,所以c(Sr2+)=3.3×10-7÷1.1×10-5=3.0×10-2=0.03mol/L。(5)若NH4SCN不再剩余的Ag+ 结合形成AgSCN白色沉淀,溶液中就会含有SCN-,就会与Fe3+产生络合物是溶液变为红色。因此滴定达到终点时溶液由无色变为血红色,且30 s不褪色。n(NH4SCN)=0.2000 mol/L×0.02L=4.0×10-3mol,所以溶液中剩余的Ag+的物质的量为n(Ag+)=4.0×10-3mol,因此与Cl―反应的Ag+的物质的量为n(Ag+)=1.100×10-2 mol -4.0×10-3mol=7.0×10-3mol n(SrCl2·6H2O)=3.5×10-3mol,m(SrCl2·6H2O)= 3.5×10-3mol×267 g/mol=0. 9345g. 所以产品纯度为0. 9345g÷1g×100%=93.45%.
考点:考查物质的制备、混合物的分离物质纯度的计算的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014学年江苏省南京市、盐城市高三第一次模拟考试化学试卷(解析版) 题型:填空题
2013年诺贝尔化学奖授予三位美国科学家,以表彰他们在开发多尺度复杂化学系统模型方面所做的贡献。可以用量子化学计算小区间内(如光合作用叶绿体光反应时酶中、生物固氮时固氮酶中)的化学反应。
(1)固氮酶有由铁蛋白和钼铁蛋白两种,它们不仅能够催化N2还原成NH3以外,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有 (不定项选择)。
a.C2H2、C2H4都是非极性分子
b.碳负离子CH3-呈三角锥形
c.NO+电子式为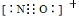

d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极也可人工合成的二价钒(V)固氮酶(结构如下图)。
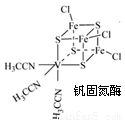
①V2+基态时核外电子排布式为 。
②钒固氮酶钒的配位原子有 (写元素符号)。
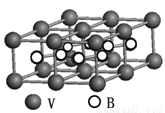
③熔融空气电池钒硼晶体晶胞结构如下图所示,该晶胞中含有钒原子数目为 。
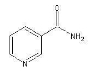
(3)烟酰胺(结构式如图)可用于合成光合辅酶NADPH ,烟酰胺分子中氮原子的杂化轨道类型有 ,1mol该分子中含σ键数目为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省茂名市高三第二次高考模拟理综化学试卷(解析版) 题型:选择题
下列陈述I、II正确并且有因果关系的是
选项 | 陈述I | 陈述II |
A | SO2和氯水有漂白性 | 两者都能使溴水褪色 |
B | 用淀粉-KI鉴别FeCl2 | Fe2+有氧化性 |
C | 盐酸和氨水能溶解Al(OH)3 | Al(OH)3是两性氢氧化物 |
D | CuSO4可以用作游泳池消毒剂 | 铜盐能使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省潮州市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
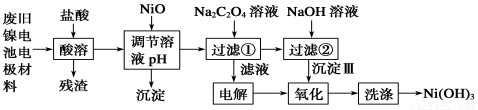
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。②K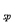 (Ni(OH)
(Ni(OH) ): 5.0×10-16 , K
): 5.0×10-16 , K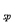 (NiC2O4): 4.0×10-10
(NiC2O4): 4.0×10-10
回答下列问题:
(1)酸溶后所留残渣的主要成份 (填物质名称)。
(2)用NiO调节溶液的pH,析出沉淀的成分为____________________(填化学式);用pH试纸测定某溶液pH的具体操作是 。
(3)写出加入Na2C2O4溶液后反应的化学方程式_____________________________。
(4)写出加入NaOH溶液所发生反应的离子方程式 ,该反应的平衡常数为 。
(5)沉淀Ⅲ可被电解所得产物之一 (填化学式)氧化生成Ni(OH)3 ,如何洗涤Ni(OH)3 沉淀?
。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省潮州市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Na2O2使酚酞溶液变红 | Na2O2能漂白织物、纸浆 |
B | SO2可使石蕊溶液先变红后褪色 | SO2的水溶液具有酸性和漂白性 |
C | NH3、HCl可用作喷泉实验 | NH3、HCl都极易溶于水 |
D | 晶体硅是良好的半导体材料 | 晶体硅可制作太阳能电池和光导纤维 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省清远市高三4月模拟理综化学试卷(解析版) 题型:选择题
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO- + H2O + 2e- = Cl- + 2OH-,关于该电池的叙述正确的是
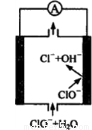
A.该电池中镁为负极,发生还原反应
B.电池工作时,OH-向正极移动
C.电池工作时,正极周围溶液的pH将不断变小
D.该电池的总反应为:Mg + ClO- + H2O = Mg(OH)2↓+ Cl-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省深圳市高三第二次调研考试理综化学试卷(解析版) 题型:填空题
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:
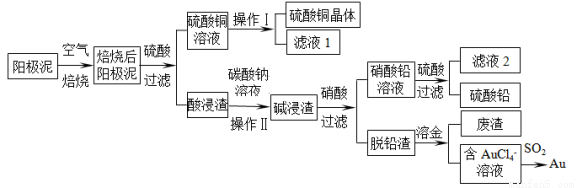
(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式)。
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标况下,11.2L乙烷中含有共价键的数目为3NA
B.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2NA
C.常温下,22.4L甲烷中含有的电子数为10NA
D.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省枣庄市高三下学期第二次模拟考试理综化学试卷(解析版) 题型:填空题
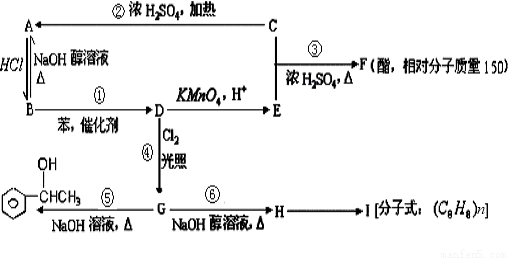
已知:苯和卤代烃在催化剂作用下可以生成烷基苯和卤化氢。根据以下转化关系(生成物中所有无机物均已略去),回答下列问题:
 。
。
(1)D的结构简式为 ,E、H中所含官能团的名称分别是 、 。
(2)①②③④⑤⑥反应中属于消去反应的是 。
(3)写出⑥的反应方程式 。
写出H→I的反应方程式 。
(4)简述验证G中含有氯元素的方法是 。
(5)写出一种符合下列要求的F的同分异构体的结构简式;
①F的同分异构体中属于酯类,能发生银镜反应,且苯环上的一氯取代物只有两种: 。
②F的同分异构体中属于醇类,能发生银镜反应,且苯环上的一氯取代物只有两种: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com