

 = ( 注:题中所涉单质均为最稳定单质)。
= ( 注:题中所涉单质均为最稳定单质)。 (2分) (2)弱于(2分)
(2分) (2)弱于(2分) 3SO2↑+ 2H2O (3分)
3SO2↑+ 2H2O (3分)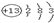 ,故答案为:
,故答案为: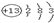 ;(2)Q是C,W是S.由其最高价氧化物对应水化合物酸性碳酸弱于硫酸推出,碳的非金属性弱于硫。(3 W的单质是硫与其最高价氧化物的水化物浓溶液是浓硫酸,共热时能发生反应,生成两种物质,其中一种是气体,根据氧化还原反应推测可知所体为二氧化硫,故反应方程式为 S + 2H2SO4(浓)
;(2)Q是C,W是S.由其最高价氧化物对应水化合物酸性碳酸弱于硫酸推出,碳的非金属性弱于硫。(3 W的单质是硫与其最高价氧化物的水化物浓溶液是浓硫酸,共热时能发生反应,生成两种物质,其中一种是气体,根据氧化还原反应推测可知所体为二氧化硫,故反应方程式为 S + 2H2SO4(浓)  3SO2↑+ 2H2O 。(4)原子序数比R多1的元素的一种氢化物(过氧化氢)能分解为它的另一种氢化物(水),故分解反应的化学方程式是2H2O2MnO22H2O + O2↑。(5)R有多种氧化物,其中甲的相对分子质量最小,则甲为NO,2L的甲气体与0.5L的氧气相混合,得到等体积的NO和NO2,由氧化还原反应可知该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐中N元素的化合价为+3价,即化学式为NaNO2,故答案为:NaNO2;(6)Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ,则C(s)+O2(g)═CO2(g)△H=-akJ?mol-1①,4Al(s)+3O2(g)═2Al2O3(s)△H=-4bkJ?mol-1②,一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则反应为4Al+3CO2=2Al2O3+3C,由盖斯定律可知,②-①×3可得到反应4Al+3CO2=2Al2O3+3C,则△H=-4bkJ?mol-1-(-akJ?mol-1)×3=(3a-4b)kJ?mol-1,故答案为:(3a-4b)kJ?mol-1.
3SO2↑+ 2H2O 。(4)原子序数比R多1的元素的一种氢化物(过氧化氢)能分解为它的另一种氢化物(水),故分解反应的化学方程式是2H2O2MnO22H2O + O2↑。(5)R有多种氧化物,其中甲的相对分子质量最小,则甲为NO,2L的甲气体与0.5L的氧气相混合,得到等体积的NO和NO2,由氧化还原反应可知该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐中N元素的化合价为+3价,即化学式为NaNO2,故答案为:NaNO2;(6)Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ,则C(s)+O2(g)═CO2(g)△H=-akJ?mol-1①,4Al(s)+3O2(g)═2Al2O3(s)△H=-4bkJ?mol-1②,一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则反应为4Al+3CO2=2Al2O3+3C,由盖斯定律可知,②-①×3可得到反应4Al+3CO2=2Al2O3+3C,则△H=-4bkJ?mol-1-(-akJ?mol-1)×3=(3a-4b)kJ?mol-1,故答案为:(3a-4b)kJ?mol-1.

科目:高中化学 来源:不详 题型:单选题

| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.元素Y、W的气态氢化物的稳定性,前者比后者差 |
| C.离子Y2-和Z3+的离子半径,后者比前者大 |
| D.元素W的最高价氧化物对应的水化物酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.M、X、Z形成的单质熔沸点 M>X>Z |
| B.氢化物的热稳定性:W>X |
| C.X分别与W和Z形成的化合物中化学键类型,晶体类型均相同 |
| D.Z元素含氧酸的酸性一定强于Y元素的含氧酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | A | |
| B | | C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若周期表中第七周期完全排满共有32种元素 |
| B.周期表中共有18个列,其中形成化合物种类最多的在第14列 |
| C.在氯化钠和氯化铯晶胞中阳离子的配位数分别为8和6 |
| D.在二氧化碳晶胞中每个二氧化碳分子周围紧邻二氧化碳分子有12个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. 6Li和7Li的电子数相等,中子数也相等 |
| B.13C和14C属于同一种元素,它们互为同位素 |
| C.1H和2H是不同的核素,它们的质子数相等 |
| D.14C和14N的质量数相等,它们的中子数不等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com