
【题目】对乙酰氨基苯酚M( ![]() )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下: 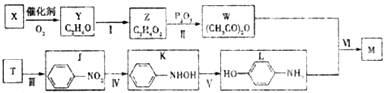
已知:①X,Y,T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色;
② ![]() .
.
(1)X,Y的结构简式为、;
(2)Ⅲ的反应类型为 , Ⅵ的反应方程式为;
(3)M与足量氢氧化钠溶液反应的化学方程式为;
(4)M有多种同分异构体,其中一类与J互为同系物且氮原子与苯环直接相连,此类同分异构体共有种; 另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应;③核碰共振氢谱有4组峰.写出其中一种同分异构体的结构简式 .
【答案】
(1)CH2=CH2;![]()
(2)取代反应;
(3)![]()
(4)9;
【解析】解:根据流程图知,X中含有两个C原子,X发生氧化反应生成Y;X,Y,T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色,则X为CH2=CH2 , X被催化氧化得到Y,根据Y分子式及核磁共振氢谱知,Y结构简式为 ![]() ;Y发生反应生成Z,根据Z分子式、W结构简式知,反应I为加成反应,Z结构简式为CH3COOH,反应II为取代反应,W结构简式为CH3COOOCCH3; T分子的核碰共振氢谱只显示1组峰,根据J结构简式知,T发生取代反应生成J,则T结构简式为
;Y发生反应生成Z,根据Z分子式、W结构简式知,反应I为加成反应,Z结构简式为CH3COOH,反应II为取代反应,W结构简式为CH3COOOCCH3; T分子的核碰共振氢谱只显示1组峰,根据J结构简式知,T发生取代反应生成J,则T结构简式为 ![]() ,结合各物质结构简式知,IV为取代反应,W和L发生取代反应生成M,(1)通过以上分析知,X、Y结构简式分别为CH2=CH2、
,结合各物质结构简式知,IV为取代反应,W和L发生取代反应生成M,(1)通过以上分析知,X、Y结构简式分别为CH2=CH2、 ![]() ,所以答案是:CH2=CH2;
,所以答案是:CH2=CH2; ![]() ;(2)通过以上分析知,III为取代反应,VI的方程式为
;(2)通过以上分析知,III为取代反应,VI的方程式为  ,所以答案是:取代反应;
,所以答案是:取代反应;  ;(3)M中肽键水解生成的羧基及M中酚羟基都能与NaOH反应,反应方程式为
;(3)M中肽键水解生成的羧基及M中酚羟基都能与NaOH反应,反应方程式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(4)M为
;(4)M为 ![]() ,M有多种同分异构体,其中一类与J互为同系物,说明含有苯环和硝基,且氮原子与苯环直接相连,如果存在﹣CH2COOH基团,有邻间对三种结构;如果存在HCOOCH2﹣基团,有邻间对三种结构,如果存在CH3CONH﹣、﹣OH基团,有邻间对三种结构,所以符合条件的有9种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应说明含有酯基;③核碰共振氢谱有4组峰,说明含有4种氢原子,符合条件的结构简式为
,M有多种同分异构体,其中一类与J互为同系物,说明含有苯环和硝基,且氮原子与苯环直接相连,如果存在﹣CH2COOH基团,有邻间对三种结构;如果存在HCOOCH2﹣基团,有邻间对三种结构,如果存在CH3CONH﹣、﹣OH基团,有邻间对三种结构,所以符合条件的有9种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应说明含有酯基;③核碰共振氢谱有4组峰,说明含有4种氢原子,符合条件的结构简式为  ,所以答案是:9种
,所以答案是:9种  ;
;


科目:高中化学 来源: 题型:
【题目】在塑料袋中放一个成熟的苹果和一些青香蕉,将袋口密封,两天后青香蕉成熟了。导致青香蕉成熟的物质是成熟苹果释放出的
A. C2H4 B. CH3COOH C. C6H6 D. CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是( )
A.常温下溶解度:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列叙述中不正确的是( )
A.在 28 g 聚乙烯树脂中,含有的碳原子个数为2NA
B.在合成 28 g 聚乙烯树脂的单体中,含有的双键数目为NA
C.28 g 聚乙烯树脂完全燃烧时,转移的电子数目为3NA
D.28 g 聚乙烯树脂中,含有的C﹣H的数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明CuSO4溶液显蓝色不是由于SO42﹣造成的,下列实验无意义的是( )
A.观察K2SO4溶液的颜色
B.加水稀释CuSO4溶液,溶液颜色变浅
C.向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色
D.向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.10gT2O含有的电子数为5NA
B.常温下,0.2L 0.5molL﹣1NH4NO3溶液的氮原子数小于0.2NA
C.用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA
D.常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液.由该废液回收铜并得到净水剂(FeCl36H2O)的步骤如下:Ⅰ.在废液中加入过量铁粉,过滤;
Ⅱ.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
Ⅲ.合并Ⅰ和Ⅱ中的滤液,通入足量氯气;
Ⅳ.…,得到FeCl36H2O晶体.
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 .
(2)试剂A是 .
(3)步骤Ⅲ中发生的离子方程式为 .
(4)完成步骤Ⅳ需要用到的实验装置是(填字母).
(5)若用FeCl36H2O晶体配制100ml 0.5mol/L的FeCl3溶液①用托盘天平称FeCl36H2O晶体,其质量是g.
②实验时下图所示操作的先后顺序为(填编号).
蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铜丝与浓硫酸反应并验证其产物性质的实验装置.
(1)①中反应的化学方程式是 , 其中铜发生了(填“氧化”或“还原”)反应,判断依据为 .
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸.加热一段时间后,③中溶液依然澄清,④中溶液褪色.想要立即终止铜与硫酸的反应,最恰当的方法是 . a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
加入试剂 | 现象 | 反应的离子方程式 | |
第一份 | 加入NaOH溶液 | 有白色沉淀生成 | |
第二份 | 加入氯水 | 有白色沉淀生成 |
完成上述反应的离子方程式.
(4)④中棉花团的作用是 .
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色.取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com