

| A.曲线I中滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.曲线I中滴加溶液到25 mL时:c(NH4+)>c(C1-)>c(H+)>c(OH-) |
| C.曲线II中滴加溶液在10 mL~25 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D.曲线II中滴加溶液到10mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |


科目:高中化学 来源:不详 题型:单选题
 SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是( )
SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是( )| A.该滴定反应可以表示为:SO32-+SO2+=2SO2 |
| B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数 |
| C.自离解的存在,说明SO2是离子化合物 |
| D.可通过导电能力变化来判断是否到达滴定终点 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该溶液一定呈酸性 |
| B.该溶液一定呈碱性 |
| C.该溶液的pH可能约为1 |
| D.该溶液的pH可能约为13 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液呈中性,可选用甲基橙或酚酞作指示剂 |
| B.溶液呈中性,只能选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 |
| D.溶液呈碱性,只能选用酚酞作指示剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1×10-11 mol·L-1,1×10-12 mol·L-1,1×10-8 mol·L-1 |
| B.1×10-11 mol·L-1,1×10-8 mol·L-1,1×10-12 mol·L-1 |
| C.2×10-11 mol·L-1,1×10-10 mol·L-1,1×10-8 mol·L-1 |
| D.1×10-8 mol·L-1,1×10-11 mol·L-1,1×10-12 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是 (填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是 (填字母)。| A.向水中加入NaHSO4 |
| B.向水中加入Cu(NO3)2 |
| C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1] |
| D.在水中加入(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①=②=③ | B.①>②=③ |
| C.①<②=③ | D.①<②<③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2(g)+3H2(g) ΔH="+49.0" kJ·mol-1
CO2(g)+3H2(g) ΔH="+49.0" kJ·mol-1 CO2(g)+2H2(g) ΔH="-192.9" kJ·mol-1
CO2(g)+2H2(g) ΔH="-192.9" kJ·mol-1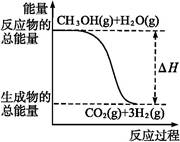
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
| B.反应①中的能量变化如上图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
D.根据②推知反应CH3OH(l)+O2(g) CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com