
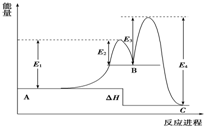
 某反应由两步反应A═B═C构成,它的反应能量曲线如图(E1、E3表示活化能).下列有关叙述正确的是( )
某反应由两步反应A═B═C构成,它的反应能量曲线如图(E1、E3表示活化能).下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 三种化合物中C最稳定 | ||
| C. | 加入催化剂会改变反应的焓变 | D. | 整个反应的△H=E1-E 2 |
分析 A.反应物总能量大于生成物总能量为放热反应,反应物总能量小于生成物总能量为吸热反应;
B.物质具有的能量越低越稳定;
C.加入催化剂改变反应途径,反应热只与始态与终态有关,与反应条件无关;
D.根据盖斯定律可知,整个反应中△H=(E1-E2)+(E3-E4)=E1+E3-E2-E4.
解答 解:A.B的能量高于A,C的能量小于B,则第一步为吸热反应,第二步为放热反应,故A错误;
B.由图可知,物质的能量B>A>C,物质具有的能量越低越稳定,则三种化合物中C最稳定,故B正确;
C.加入催化剂改变反应途径,反应热只与始态与终态有关,与反应条件无关,催化剂不影响反应热,故C错误;
D.根据盖斯定律可知,整个反应中△H=(E1-E2)+(E3-E4)=E1+E3-E2-E4,故D错误,
故选:B.
点评 本题考查化学反应与能量变化,题目难度中等,注意把握物质的总能量与反应热的关系,易错点为D,注意把握反应热的计算.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、SO42-、Cl- | B. | K+、OH-、HCO3- | C. | Mg2+、SO42-、Cl- | D. | Cu2+、H+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
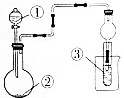 利用如图所示装置进行下列实验,不能得出相应实验结论的是( )
利用如图所示装置进行下列实验,不能得出相应实验结论的是( )| 选项 | ① | ② | ③ | ③中的现象 |
| A | 浓盐酸 | Na2SO3 | BaCl2溶液 | 出现浑浊 |
| B | 稀盐酸 | 石灰石 | 饱和Na2CO3溶液 | 出现浑浊 |
| C | 浓氨水 | 生石灰 | 酚酞溶液 | 出现红色 |
| D | 醋酸 | 贝壳 | 澄清石灰水 | 先浑浊后澄清 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 节约能源,提高能源利用率 | |
| B. | 大量开采化石原料,以满足社会对能源的要求 | |
| C. | 减少直至不使用对大气臭氧层起破坏作用的氟氯烃 | |
| D. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| C. | 用于食品包装的塑料制品,属于热塑性塑料,可回收再利用 | |
| D. | 聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com