

| A. | 甲装置为铁的析氢腐蚀,若将铁换成铜,则甲装置就是铜的吸氧腐蚀 | |
| B. | 若将甲装置中的电流表改为电源,无论电源怎么连接,C电极上都会有气体放出 | |
| C. | 乙装置中K关闭后,a极附近颜色逐渐加深变黑 | |
| D. | 若将乙装置中的NaOH溶液换为HCl溶液,则K关闭后b极颜色变浅 |
分析 A.铜与盐酸不反应,形成原电池反应时发生吸氧腐蚀;
B.C电极若为阳极,则溶液中Cl-放电,生成Cl2,若C电极为阴极,则溶液中的H+放电生成H2;
C.硫化银胶粒带负电荷,向阳极移动;
D.若将乙装置中的NaOH溶液换为HCl溶液,因为镁比铝活泼,所以镁为负极.
解答 解:A.因为铁是氢前金属,所以甲装置为铁的析氢腐蚀,若将铁换成铜,因为铜是氢后金属,则甲装置就是铜的吸氧腐蚀,故A正确;
B.若将甲装置中的电流表改为电源,C电极若为阳极,则溶液中Cl-放电,生成Cl2,若C电极为阴极,则溶液中的H+放电生成H2,故B正确;
C.乙装置中K关闭后,因为Al能与NaOH溶液反应,所以Al为负极,则a为阴极,b为阳极,硫化银胶体属于金属硫化物是带负电的胶体粒子,所以移向阳极,故a极附近颜色逐渐加深变黑是错误的,故C错误;
D.若将乙装置中的NaOH溶液换为HCl溶液,因为镁比铝活泼,所以镁为负极,则a为阳极,b为阴极,则K关闭后硫化银胶体移向a极,b极颜色变浅正确.故D正确.
故选C.
点评 本题考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池的工作原理,答题时注意:(1)电池问题的解决要以确定电极为第一步,然后按照电极反应的特点进行分析;(2)胶体粒子带电的规律是金属氧化物和金属的氢氧化物带正电,金属硫化物和非金属氧化物带负电,题目难度不大.


 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | 箭头上为反应条件或试剂 | 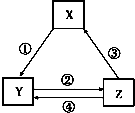 |
| A | Fe | FeCl2 | FeCl3 | ①通入少量Cl2 | |
| B | Na2CO3 | NaCl | NaHCO3 | ②先通CO2、再通过量NH3 | |
| C | SiO2 | Na2SiO3 | H2SiO3 | ③加热 | |
| D | NaAlO2 | Al(OH)3 | Al2O3 | ④加H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不可能生成90g 乙酸乙酯 | B. | 生成的乙酸乙酯中含有18O | ||
| C. | 可能生成61.6g 乙酸乙酯 | D. | 生成的水分子中一定含有18O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
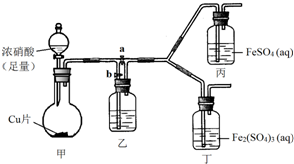 某学生欲通过实验方法验证Fe2+的性质.
某学生欲通过实验方法验证Fe2+的性质.| 实验操作 | 预期现象 | 反应的离子方程式 |
| 向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO${\;}_{3}^{-}$+2H+=Fe3++NO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
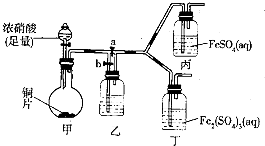
| 实验操作 | 预期现象 | 离子方程式 |
| 向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO3-+2H+=Fe3++NO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅酸钠可用作木材防火涂料 | B. | Fe2O3可用作外墙涂料 | ||
| C. | 过氧化钠可用作潜艇供氧剂 | D. | 铝制容器可以贮运稀硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com