
| A. | Fe和浓硫酸 | B. | Fe和浓硝酸 | C. | Al和浓硫酸 | D. | Al和浓硝酸 |
分析 硝酸、浓硫酸都具有强氧化性,能与金属发生氧化还原反应,而常温下,Fe、Al遇浓硫酸或浓硝酸发生钝化,阻止反应进一步发生,以此来解答.
解答 解:浓硝酸、浓硫酸都具有强氧化性,在常温下,金属铁或金属铝遇到浓硝酸会在金属表面形成致密的氧化膜发生钝化,
A.常温下Fe和浓硫酸表面形成致密的氧化膜,发生钝化反应,故A正确;
B.常温下Fe和浓硝酸金属表面形成致密的氧化膜,发生钝化反应,故B正确;
C.常温下Al和浓硫酸金属表面形成致密的氧化膜,发生钝化反应,故C正确;
D.常温下金属Al与浓硝酸发生钝化反应,会在金属表面形成致密的氧化膜,故D正确;
故选ABCD.
点评 本题考查金属钝化的有关知识,明确发生钝化的金属只有Al、Fe,酸为浓硝酸、浓硫酸是解答本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 中性溶液中:Fe3+、Cl-、Na+、SO42- | |
| B. | pH=1的溶液中:NO3-、K+、CO32-、Br- | |
| C. | 紫色石蕊呈蓝色的溶液中:S2-、Na+、SO32-、I- | |
| D. | 焰色反应为黄色的溶液中:CH3COO-、NH4+、AlO2-、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
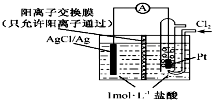 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )| A. | 正极反应为AgCl+e-=Ag+Cl- | |
| B. | 电池工作时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 若用KCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、D2、T2互为同素异形体 | |
| B. | 液氨、氨水、王水都是混合物 | |
| C. | H2O、苯酚、Fe(SCN)3都是弱电解质 | |
| D. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
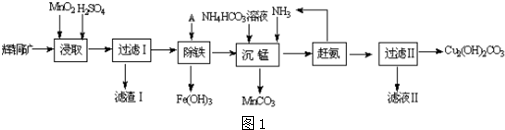
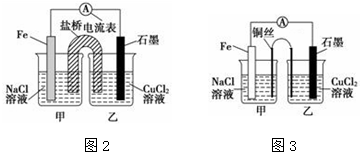
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 中和滴定达中点时俯视滴定管内液面度数 | |
| B. | 碱式滴定管用蒸馏水洗净后立即装待测溶液来滴定 | |
| C. | 酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 | |
| D. | 把配好的标准溶液倒入刚用蒸馏水洗净的锥形瓶中然后用来滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人们可以把放热反应释放的能量转化为其它可利用的能量,而吸热反应没有利用价值 | |
| B. | 太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用 | |
| C. | 地球上最基本的能源是化学能 | |
| D. | 利用二氧化碳制造全降解塑料能有效减少“白色污染” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ①②③④ | D. | ①②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com