
����Ŀ�����������һ���������������Ⱦ�Ϲ�ҵ��ij��ȤС�����Ʊ�Ca��NO3��2���������ʽ���̽���� �������زġ�
��NO+NO2+Ca��OH��2=Ca��NO3��2+H2O
��Ca��NO3��2�ܱ�����KmnO4��Һ������NO3�� �� MnO4������ԭΪMn2+
�������������£�Ca��NO3��2�ܽ�I������ΪI2 �� S2O32���ܽ�I2��ԭΪI��
���Ʊ��������
��1������ͬѧ��������ͼ��ʾװ���Ʊ�������� 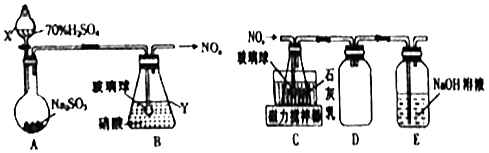
������X��Y�����Ʒֱ����� ��
��װ��B���ݳ���NO��NO2�����ʵ���֮��Ϊ1��1����װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2�����Ʊ�Ca��NO2��2�� ����ͬѧ������װ��B�в����ĵ��������Ʊ�Ca��NO2��2 �� װ��������ͼ��
��װ��C�е���ĩ�˽�һ������������� ��
��װ��D����������װ��E�������� ��
��3�����ⶨCa��NO2��2�Ĵ��ȡ� ����ͬѧ��ⶨCa��NO2��2�Ĵ��ȣ����ʲ��μӷ�Ӧ�����ɹ�ѡ����Լ���
a��ϡ���� b��c1molL��1��KI��Һ c��������Һ d��c2molL��1��Na2S2O3��Һe��c3molL��1������KMnO4��Һ
������Ca��NO2��2�Ļ�ԭ�����ⶨ���䴿�ȣ���ѡ����Լ���������ĸ����
������Ca��NO2��2�����������ⶨ�ȵIJ��裺ȷ��ȡmgCa��NO2��2��Ʒ������ƿ�У�������ˮ�ܽ⣬���벹������ʵ�鲽�裩
���𰸡�
��1����Һ©������ƿ��2SO2+H2O+2HNO3=NO+NO2+2H2SO4
��2��������ʯ����ĽӴ������������������δ��Ӧ�ĵ�������
��3��e�����������c1mol?L��1KI��Һ��������Һ��Ȼ��μ�ϡ���ᣬ��c2mol?L��1Na2S2O3��Һ�ζ�����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ����ȡ���ĵ�Na2S2O3��Һ������ظ����ϲ���2��3��
���������⣺��1���������������֪XΪ��Һ©����YΪ��ƿ�� ���Դ��ǣ���Һ©������ƿ����װ��B���ݳ���NO��NO2�����ʵ���֮��Ϊ1��1����װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ2SO2+H2O+2HNO3=NO+NO2+2H2SO4�����Դ��ǣ�2SO2+H2O+2HNO3=NO+NO2+2H2SO4����2����װ��C�е���ĩ�˽�һ�������������ʯ����ĽӴ������
���Դ��ǣ�������ʯ����ĽӴ��������װ��D�������Ƿ�������Eװ����������������δ��Ӧ��ĵ��������ֹ��Ⱦ������
���Դ��Ƕ������������δ��Ӧ�ĵ��������3��������ϢCa��NO2��2�ܱ�����KmnO4��Һ������NO3�� �� MnO4������ԭΪMn2+��֪��������Ca��NO2��2�Ļ�ԭ�����ⶨ�䴿�ȣ���ѡ����Լ���e��
���Դ��ǣ�e��������Ϣ�����������£�Ca��NO3��2�ܽ�I������ΪI2 �� S2O32���ܽ�I2��ԭΪI����֪��������Ca��NO2��2�����������ⶨ�䴿�ȵIJ����ǣ�ȷ��ȡ����Ϊm��Ca��NO2��2��Ʒ������ƿ�У�������ˮ�ܽ⣬���������c1 molL��1 KI��Һ��������Һ��Ȼ��μ�ϡ���ᣬ��c2 molL��1 Na2S2O3��Һ�ζ�����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ����ȡ���ĵ�Na2S2O3��Һ������ظ����ϲ���2��3�Σ�
���Դ��ǣ����������c1 molL��1 KI��Һ��������Һ��Ȼ��μ�ϡ���ᣬ��c2 molL��1 Na2S2O3��Һ�ζ�����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ����ȡ���ĵ�Na2S2O3��Һ������ظ����ϲ���2��3�Σ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ڵ�������ܵ�����ǣ�������
A.��ˮB.����C.����D.���ڵ��Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����ͼ��ʾA��B��C������������ѡ�������������Ƶ���ţ�������Ӧ�Ŀո��ڣ����ձ�������ͨ©������Բ����ƿ������ƿ���ݷ�Һ©����
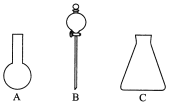
A________��B________��C________��
(2)ijͬѧ��������ƽ�����ձ�����������ƽƽ����״̬����ͼ��ʾ����ͼ�п��Կ�������ͬѧ�ڲ���ʱ��һ��������______________________________���ձ���ʵ������Ϊ________g��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β����Ⱦ�����������������Ҫԭ��֮һ����������������������������⣬����Ҫ�����з�������β����ת���������ü����д����������ѡ������ǹؼ���ijϡ��������ת������β��ʾ��ͼ��ͼ�� 
��1�������й�˵����ȷ���� �� a��C3H8��CH3CH=CH3һ����������̼ԭ�Ӷ����õ���SP3�ӻ�
b��N2��CO2��H2O���ǷǼ��Է���
c��ÿ��CO2�����У�����2���м���2���Ҽ�+
d��CO��һ�ֵȵ�����ΪNO+ �� ���ĵ���ʽΪ ![]()
��2��CO��Fe�������ʻ���[Fe��CO��5]����֪������Ϊ0�ۣ���ԭ�ӵĻ�̬��������Ų�ʽΪ �� [Fe��CO��5]������λԭ���� �� ������ ��
��3��C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳���� �� Al2O3�����۵�����ͻ���ϣ�AlCl3�������������۵�ͣ���ҵ�ϵ�ұ��ȡ����ǰ�߶����ú��ߵ�ԭ���� ��
��4�����ѿ��ͷ���������Ҳ����Ϊ����β��ת���Ĵ�����һ�ָ��������ᄃ���ṹ��ͼ����ʾ������ÿ��Sr2+����O2�����ڣ���Sr2+�����O2���ĺ˼��Ϊapm�������ӵ�����ΪNA �� ��������ᄃ���ܶȵļ������ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л�������A��C5H8O2��������ˮ�������Է�����ͼ��ʾ�ı仯 
��֪��C���ʵ�һ�ȴ���Dֻ������ͬ���칹�壬��ش�
��1��A�����к��еĹ����ŵ�����
��2���٢ڢܢݷ�Ӧ������ȡ����Ӧ����������ţ���
��3��д���ڵķ�Ӧ����ʽ ��
��4��д��һ������Ҫ������ʵ�ͬ���칹��Ľṹ��ʽ ��C��ͬ���칹�������������ܷ���������Ӧ ��
��C��ͬ���칹�������ڴ����ܷ���������Ӧ ��
��5��������֤D�к�����Ԫ�صķ��� ��
��6��17.2g B��������̼��������Һ��Ӧ����״�������ɶ�����̼�����ΪL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
P4�����ף�s��+5O2��g���TP4O10��s����H=��2983.2kJ/mol
P�����ף�s��+ ![]() O2��g���T
O2��g���T ![]() P4O10��s����H=��738.5kJ/mol
P4O10��s����H=��738.5kJ/mol
��д������ת��Ϊ�����Ȼ�ѧ����ʽ�������ȶ��ԱȺ�������ߡ��͡�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ͼ����ʾΪ��άƽ�澧��ʾ��ͼ����ѧʽ��ʾΪAX3����________��
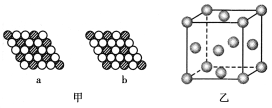
(2)ͼ��Ϊһ������ͭ�ľ�������������¸��⣺
�ٸþ�����ʵ�ʡ�ӵ�е�ͭԭ������________����
�ڸþ�����Ϊ________(�����)��
A���������� B�������������� C��������������
�۴˾���������ı߳�Ϊa cm��Cu�����ԭ������Ϊ64������ͭ���ܶ�Ϊ�� g/cm3�����ӵ�����Ϊ________(��a�ѱ�ʾ)��
(3)��X���߽���ѧ���м��ع���ͭ�����γ���������Ľ����������ṹ����ͼ��ʾ�������й�˵����ȷ����________��
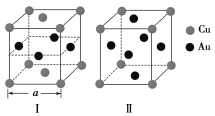
A��ͼ�������ʵĻ�ѧʽ��ͬ
B��ͼ�������ʵĻ�ѧʽΪCuAu3
C��ͼ������ÿ��ͭԭ�ӽ��ڵ�ͭԭ����3��
D����ͼ���о����ı߳�Ϊa cm����ͼ���кϽ���ܶ�Ϊ![]() g��cm��3
g��cm��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.��H2O��ͨ�� NO2��3NO2+H2O�TH++NO3��+2NO
B.��Na2SiO3��Һ��ͨ������SO2��Na2SiO3+SO2+H2O�TH2SiO3��+2Na++SO32��
C.�ñ��ʹ��p��Һϴ���Թ��в����ı��ӣ�CO32��+2 ![]() ��2
��2 ![]() +CO2��+H2O
+CO2��+H2O
D.����������ʵ���Ũ�ȵ�NH4Fe��SO4��2��Ba��OH��2��ϣ�2Fe3++3SO42��+3Ba2++6OH���T3BaSO4��+2Fe��OH��3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com