
【题目】下列离子方程式表达正确的是
A. 硫化钠的水解反应:S2-+H3O+![]() HS-+H2O
HS-+H2O
B. 用铜作阳极电解氯化铜溶液:Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
C. Na2CO3溶液呈碱性的原因:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
D. 在Ba(OH)2溶液中滴加KHSO4溶液至pH=7:Ba2++OH-+H++SO42-=BaSO4↓+H2O
【答案】C
【解析】
A.S2-水解,消耗水电离产生的H+,使溶液显碱性,离子方程式为S2-+H2O![]() HS-+OH-,A错误;
HS-+OH-,A错误;
B.用Cu作阳极,阳极发生氧化反应,Cu-2e-=Cu2+,在阴极上溶液中的氢离子得到电子变为H2,故电解总反应方程式为Cu+2H2O![]() Cu(OH)2+H2↑,B错误;
Cu(OH)2+H2↑,B错误;
C.Na2CO3是强碱弱酸盐,在溶液中CO32-发生水解反应,消耗水电离产生的H+,使溶液显碱性,用离子方程式表示为:CO32-+H2O![]() HCO3-+OH-,C正确;
HCO3-+OH-,C正确;
D.在Ba(OH)2溶液中滴加KHSO4溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
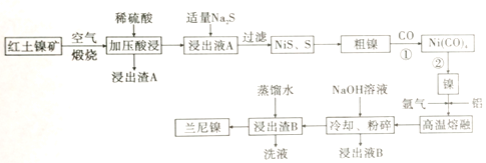
(1)煅烧时生成的主要气体产物是________ ,浸出渣A的主要成分是________。
(2)红土镍矿煅烧后生成的Ni2O3有强氧化性,加压酸浸时有无色无味的气体产生且有NiSO4生成,则该反应中氧化产物与还原产物的物质的量之比为________。
(3)向浸出液A中加入适量Na2S,发生氧化还原反应的离子方程式为________。
(4)若Na2S过量,则过滤出的固体中会混有________;H2S也可代替Na2S使用,但不利之处是________。
(5)已知Ni(CO)4的沸点是42.2℃,Ni(s)+CO(g) ![]() Ni(CO)4(g)的平衡常数与温度关系如下:
Ni(CO)4(g)的平衡常数与温度关系如下:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
步骤①、步骤②的最佳温度分别是________、 ________(选填项代号)。
A.25℃ B.30℃ C.50℃ D.80℃ E.230℃
(6)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备,熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来室内装修材料释放出的甲醛、苯、氨等有害气体严重影响人体健康,工业上利用氨气与甲醛(HCHO)的反应,不仅可消除污染,还可生产重要的工业原料六亚甲基四胺(结构如图所示,另一种产物是水)。下列有关说法错误的是
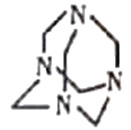
A.六亚甲基四胺的分子式为C6H12N4
B.六亚甲基四胺分子的摩尔质量为140 g·mol-1
C.参与反应的氨气与甲醛的物质的量之比为2:3
D.反应涉及的4种物质均为非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用作晒制蓝图。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置可重复选用)进行实验:

①E中盛装碱石灰的仪器名称为_________。
②按照气流从左到右的方向,上述装置的接口顺序为a→g→f→_____→尾气处理装置(仪器可重复使用)。
③实验前先通入一段时间N2,其目的为__________________。
④实验证明了气体产物中含有CO,依据的实验现象为_____________。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为____________________。
(3)晒制蓝图时,以K3[Fe(CN)6]溶液为显色剂,该反应的化学方程式为______________。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀HSO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用 cmol/L KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用 cmol/L KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为______________;步骤3中加入锌粉的目的为_______。
(5)草酸亚铁晶体样品的纯度为________;若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将____(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程与氧化还原反应无关的是
|
|
|
|
A. 工业上原油的分馏 | B. 生活中用“暖宝宝”取暖 | C. 拉瓦锡测定空气中O2含量 | D. 普利斯特利光合作用实验 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,向1.0L恒容密闭容器中充入1.0mol SO3气体,发生反应:2SO3(g)![]() 2SO2(g)+O2(g) △H=+196 kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6kJ的热量。当温度不变时,改变某一条件时,下列结论正确的是
2SO2(g)+O2(g) △H=+196 kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6kJ的热量。当温度不变时,改变某一条件时,下列结论正确的是
条件改变 | 结论 | |
A | 平衡后的容器中充入1.0molHe | 平衡逆向移动,化学平衡常数减小 |
B | 起始时向容器中充入1.0molSO2 和0.50molO2 | 达到平衡时共放出78.4kJ的热量 |
C | 起始时向容器中充入2.0 molSO3、0.50 molSO2和0.25 mol O2 | 反应达到平衡前v(正)>v(逆) |
D | 起始向容器中充入2.5 molSO2 和1.25molO2 | 达到平衡时,SO2的转化率为80.0% |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制取乙炔的化学方程式为_________________,检验产物乙炔时需要用________溶液(填化学式),用_________溶液除去杂质气体H2S、PH3;实验室制取乙烯检验产物时,用溴水或酸性高锰酸钾检验乙烯时都需要除去________(写化学式,下同)的干扰;溴乙烷发生消去反应时用酸性高锰酸钾溶液检验产物时是否需要除杂,请简述原因_________________________________________。
(2)请对以下过程形成的分散系进行分类:①花生油加入到水中后充分搅拌;②向蒸馏水中加入硝酸钾至恰好饱和;③饱和氯化铁溶液中逐滴加入少量氢氧化钠溶液;④氢氧化钡溶液中通入过量的CO2;⑤用滤纸过滤氢氧化铁胶体后得到的滤液; ⑥将纳米材料分散在塑料中制备复合材料;⑦碘水和酒精的混合物。属于胶体的是____________,一般通过_______________现象鉴别胶体。
(3)取2.08g某NaHSO3(摩尔质量为104g/mol)样品,溶于水,再转移到100mL容量瓶中,用蒸馏水定容;取出5mL,并用0.01mol/L KMnO4酸性溶液滴定(产物为Mn2+),用去10.00mL,写出滴定过程中发生反应的离子方程式____________,该样品的纯度为_______
(4)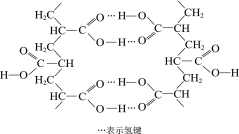 ,单体的结构简式为__________________
,单体的结构简式为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是钢铁在海水中的锈蚀过程,以下有关说法正确的是( )
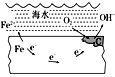
A. 该金属腐蚀过程为析氢腐蚀B. 正极为C,发生的反应为氧化反应
C. 该金属腐蚀过程是吸氧腐蚀D. 负极的反应式为O2+2H2O+4e-===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。
下列说法错误的是( )
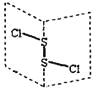
A. S2Cl2的结构式为Cl-S-S-Cl
B. S2Cl2为含有极性键和非极性键的非极性分子
C. S2Br2与S2Cl2结构相似,分子间作用力:S2Br2>S2Cl2
D. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com