

���� ��1��SO2ͨ��NaOH��Һ�����ݵ���غ���c��Na+��+c��H+��=c��HSO3-��+2c��SO32-��+c��OH-�����ݴ˴��⣻
��2����SO2ͨ������ƣ�Na2C2O4����NaOH�Ļ����Һ����Na2S2O4������Ԫ���غ��֪���ﻹ��̼���ƺ�ˮ�����ݵ���غ���д���ӷ���ʽ��
��3������������������Ϣ����ҵ����Na2S��Na2CO3�Լ�SO2��ȡNa2S2O3������Ԫ���غ��д����Ӧ�Ļ�ѧ����ʽ��
������Ϊ��Լ�ɱ������ٶԻ�������Ⱦ�����Խ�������������ĸҺѭ��ʹ�ã����ݷ�Ӧ����ʽ��Ͷ�������֮�ȵȷ�Ӧ�еļ�����֮�ȣ���SO2����������߲��ʣ��ݴ˴��⣻
������Na2CO3��Һ���������Ӧ�������������ƣ��������ƿɱ������������ƣ��Ƚ�Na2S2O3��Na2SO3��Na2SO4�Ļ�ѧʽ��֪��Na2S2O3��Na2SO3��Na2SO4������������ԭ������ԭ�����ʵ���֮�Ȳ�ͬ����Na2SO3��Na2SO4����ԭ������ԭ�����ʵ���֮����ͬ����Na2S2O3��Na2SO3����ԭ������ԭ�����ʵ���֮����ͬ��Na2S2O3����ԭ������ԭ�����ʵ���֮�Ƚ���Na2SO3��Na2SO4֮�䣬�ݴ�ѡ��
��4���ٸ��ݵ��ӵ�ʧ�غ���㱻SO2��ԭ��O2��������
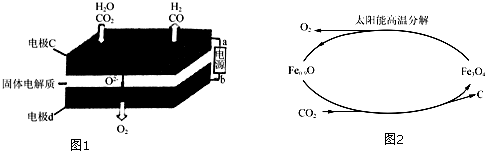
��ͼ�е�װ��Ϊ���أ�������ͭ���ӵõ�������ͭ�������϶�������ʧ����������������ӣ�
��� �⣺��1��SO2ͨ��NaOH��Һ�����ݵ���غ�ɵã�c��Na+��+c��H+��=c��HSO3-��+2c��SO32-��+c��OH-��������c��Na+��+c��H+����c��HSO3-��+c��SO32-��+c��OH-������������������С��������������
�ʴ�Ϊ��D��
��2����SO2ͨ������ƣ�Na2C2O4����NaOH�Ļ����Һ����Na2S2O4������Ԫ���غ��֪���ﻹ��̼���ƺ�ˮ����Ӧ�����ӷ���ʽΪ��2SO2+C2O42-+4OH- $\frac{\underline{\;\;��\;\;}}{\;}$S2O42-+2CO32-+2H2O��
�ʴ�Ϊ��2SO2+C2O42-+4OH- $\frac{\underline{\;\;��\;\;}}{\;}$S2O42-+2CO32-+2H2O��
��3������������������Ϣ����ҵ����Na2S��Na2CO3�Լ�SO2��ȡNa2S2O3����Ӧ�Ļ�ѧ����ʽΪ4SO2+2Na2S+Na2CO3$\frac{\underline{\;ͨ��\;}}{\;}$3Na2S2O3+CO2��
�ʴ�Ϊ��4SO2+2Na2S+Na2CO3$\frac{\underline{\;ͨ��\;}}{\;}$3Na2S2O3+CO2��
������Ϊ��Լ�ɱ������ٶԻ�������Ⱦ�����Խ�������������ĸҺѭ��ʹ�ã����ݷ�Ӧ����ʽ��Ͷ�������֮�ȵȷ�Ӧ�еļ�����֮�ȣ���SO2����������߲��ʣ�������ȡ���������֡�ӯ������Լ�ɱ������ٶԻ�������Ⱦ�������ܵ���߲��ʡ���һ˼����У��٢ۢݣ�
�ʴ�Ϊ���٢ۢݣ�
������Na2CO3��Һ���������Ӧ�������������ƣ��������ƿɱ������������ƣ�����������Na2SO3��Na2SO4���Ƚ�Na2S2O3��Na2SO3��Na2SO4�Ļ�ѧʽ��֪��Na2S2O3��Na2SO3��Na2SO4������������ԭ������ԭ�����ʵ���֮�Ȳ�ͬ����Na2SO3��Na2SO4����ԭ������ԭ�����ʵ���֮����ͬ����Na2S2O3��Na2SO3����ԭ������ԭ�����ʵ���֮����ͬ��Na2S2O3����ԭ������ԭ�����ʵ���֮�Ƚ���Na2SO3��Na2SO4֮�䣬���Ը��ݲ�Ʒ����ԭ�Ӻ���ԭ�ӵ����ʵ���֮�ȿ�ȷ��Na2S2O3�����ʵ�����������ѡA��
�ʴ�Ϊ��Na2SO4��A��
��4�����ڷ�Ӧ��2SO2+2n Cu+��n+1��O2+��2-2n�� H2O=2n CuSO4+��2-2n�� H2SO4 �У�ÿĦ����������ʧȥ2mol���ӣ���ÿĦ�������ܵõ�4mol���ӣ�����1molSO2�ܻ�ԭ0.5molO2��ÿ���ձ�״����11.2L��0.5molSO2����SO2��ԭ��O2������Ϊ��0.25mol��32g/mol=8g��
�ʴ�Ϊ��8��
��ͼ�е�װ��Ϊ���أ�������ͭ���ӵõ�������ͭ�������϶�������ʧ����������������ӣ���Ӧ����ʽΪCu2++SO2+2H2O$\frac{\underline{\;���\;}}{\;}$ Cu+SO42-+4H+��
�ʴ�Ϊ��Cu2++SO2+2H2O$\frac{\underline{\;���\;}}{\;}$Cu+SO42-+4H+��
���� ������Ҫ����Ԫ�ػ�����֪ʶ�빤ҵӦ�ã���Ŀ�Ѷ��еȣ������漰֪ʶ��϶ࡢ�ۺ���ǿ������ʱע��Ԫ�ػ��������֪ʶ�ͻ�ѧԭ��֪ʶ��������ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BiԪ�ص���������209 | |
| B�� | BiԪ�����������Ļ�ѧʽΪBi2O3 | |
| C�� | BiԪ��λ��Ԫ�����ڱ��������ڵ�VA�� | |
| D�� | BiΪ������Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 +4NaOH$��_{��}^{����Һ}$NaOOCC��CCOONa+2NaBr+4H2O��
+4NaOH$��_{��}^{����Һ}$NaOOCC��CCOONa+2NaBr+4H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��Ԫ�ص��������ض���ͬ | |
| B�� | ��ͬԪ��ԭ�ӵ��������ض���ͬ | |
| C�� | ԭ�Ӻ˶��������Ӻ����ӹ��ɵ� | |
| D�� | ���Ǻ����������ͬ�����ض�����ͬһԪ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ�ÿ�������Դ���ó��ٽ������̼����л��ܼ���ע��ԭ�ӵľ����ԡ����õ��ܺ��������ն�������ɫ��ѧ��˼�� | |
| B�� | ���ִ���ѧ��ҵ�д�����Ӧ��ʮ���ձ飬���ڸ��������·�Ӧ��֮���ܹ�ͬʱ���������Ӧʱ��������������Դ�������Ŀ����������ղ����еı��� | |
| C�� | ʯ���ѽ⡢ú�����������ϻ�����ˮ��þ�������绯����ά���ƻ��ȹ����ж�������ѧ�仯 | |
| D�� | PM2.5��ָ������ֱ��С�ڻ����2.5�Ŀ����Ҳ��Ϊ��ϸ�������PM2.5�ڿ�����ֻ�γ����ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��COC12�׳ƹ�����������Cԭ�Ӳ�ȡsp2�ӻ��ɼ����������ӵĽṹʽΪ
��1��COC12�׳ƹ�����������Cԭ�Ӳ�ȡsp2�ӻ��ɼ����������ӵĽṹʽΪ ������̼��ԭ��֮�乲�ۼ���c������ţ���
������̼��ԭ��֮�乲�ۼ���c������ţ��� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol | B�� | 2mol | C�� | 2.5mol | D�� | 10mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ཫ̫����ת��Ϊ���ܵij��ò��� | |
| B�� | ���ṤҵNOѭ�����ã�������ÿĦ������������1Ħ������ | |
| C�� | ��ͨʳ���к���3%��5%�Ĵ��� | |
| D�� | �ձ���й©����53131Iԭ�ӣ����������� 55134Cs����������2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com