
现有A.B.C三种化合物,各取40g相混合,完全反应后,得B18g,C49g,还有D生成。已知D的式量为106。现将22gA和11gB反应,能生成D ( )
A.1mol B. 0.5mol C. 0.275mol D. 0.25mol
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 元素编号 | a | b | c | d | e | f | g | h | i |
| 原子半径/nm | 0.037 | 0.064 | 0.073 | 0.070 | 0.088 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或 最低化合价 |
+1 | -1 | -2 | -3 | +3 | -2 | +3 | +1 | +1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省八校高三第二次联考理综化学试卷(解析版) 题型:填空题
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:
Ⅰ.(1)C、D、E元素的第一电离能由大到小的关系为____________。(用相应的元素符号表示)
(2)请比较C2A4、D2A4、G2A4三种化合物的沸点由高到低的顺序为??? ____________________。(用化学式表示)
(3)有某种分子式为C4D4E8的物质(该物质中同种原子的化学环境完全相同,不含碳碳双键)是一种威力极强的炸药,则可推知其结构简式为____________。
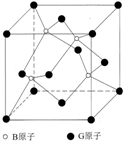
Ⅱ.BG是一种耐磨材料,其与金刚石结构相似,右图为其结构中的最小重复单元,它可由B的三溴化物和G的三溴化物于高温下在氢气的氛围中合成。
(1)指出B的三溴化物中B的杂化方式为___________;G的三溴化物分子的结构为_________型。
(2)写出合成BG的化学反应方程式为_______________________________。
(3)已知晶体中B与G原子的最近距离为a pm,则该晶体的密度的表达式为__________g/cm3。(不需化简)
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江省高二下学期期末考试化学试卷(解析版) 题型:填空题
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同
B元素原子的核外p电子总数比s电子总数少1
C原子p轨道上成对电子数等于未成对电子数,且与A同周期
D元素的族序数与周期数的差为4,且不与A元素在同一周期
E位于周期表中第七列
F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子
(1)A的基态原子最外层有 种不同运动状态的电子,F位于 区。
(2)E2+的基态核外电子排布式为 ,AD4为 (填极性或非极性)分子。
(3)A、B、C三种元素的电负性由小到大的顺序是 (用元素符号表示),B和C两元素中,B的第一电离能较大的原因是 ,与AC2互为等电子体的分子的名称为 。(只写一种)
(4)BD3 中心原子的杂化方式为 ,其分子空间构型为 。
(5)用晶体的x射线衍射法对F的测定得到以下结果:F的晶胞为面心立方最密堆积(如图),又知该晶体的密度为ρg/cm3,晶胞中该原子的配位数为 ;F的原子半径是 pm;(阿伏加德罗常数为NA)。

查看答案和解析>>
科目:高中化学 来源:2013届河北省五校联盟高三上学期调研考试理科综合化学试卷(解析版) 题型:填空题
【化学—选修5:物质结构与性质】(15分)
现有A、B、C、D、E原子序数依次增大的五种元素,它们位于元素周期表的前四周期。A元素原子的价层电子总数是内层电子总数的2倍;C元素原子的L电子层中只有两对成对电子;D元素与E元素在同周期相邻的族,它们的原子序数相差3,且D元素的基态原子有4个未成对电子。请回答下列问题:
⑴A、B、C三种元素的名称分别为 、 、 。
⑵用元素符号表示A、B、C三种元素的第一电离能由低到高的排序为 。
⑶E元素基态原子的核外电子排布式为 。
⑷A元素与氢元素能形成种类繁多的化合物,其中只含sp3杂化且相对分子质量最小的分子的VSEPR空间构型为 ;其中只含sp2杂化且相对分子质量最小的化合物的结构式为 ;其中同时含sp杂化、SP2杂化、sp3杂化且相对分子质量最小的化合物的化学式为 。
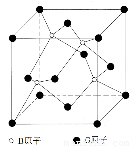
⑸A元素的一种单质的晶体结构如图甲所示,D元素的一种单质的晶体结构如图乙所示。


图甲中A原子的配位数与图乙中D原子的配位数之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com