
| 组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
| C(KI) | V | C(H2SO4) | V | ||||
| 1 | 25℃ | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | l组和2组探究②温度对该反应速率的影响;2组和3组探究反应物浓度对该反应速率的影响 |
| 2 | 35℃ | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | |
| 3 | 35℃ | 1mol/L | 5mL | ①0.2mol/L硫酸 | 5mL | 3滴 | |
| 实验方案 | 预期实验现象与结论 |
| 取少量碘水于试管中,滴入几滴淀粉溶液,然后逐滴加入1mol/L KOH溶液,观察现象. | 若蓝色不褪色,则假设二正确. |
分析 KI中-1价的碘离子具有还原性,氧气具有氧化性,两者发生氧化还原反应,生成碘单质和水,结合原子守恒和电荷守恒书写离子方程式.
(1)根据表格,对比①②的数据,可以看出实验①②是探究温度对反应速率的影响;实验①③是探究反应物浓度对该反应速率的影响,所以此时两个实验中H2SO4溶液应当不相等,据此答题;
(2)实验中应先向一定体积的KI溶液中滴加淀粉溶液,然后再加入稀硫酸,在酸性条件下发生氧化还原反应生成碘,应记录的数据为反应的时间;
(3)淀粉与碘水作用显蓝色,加入氢氧化钾,若蓝色不褪色,说明溶液中溶液碱性弱,I2和KOH不反应.
解答 解:KI中-1价的碘离子具有还原性,氧气具有氧化性,两者发生氧化还原反应,反应的离子方程式为:O2+4I-+4H+=212+2H2O,
故答案为:O2+4I-+4H+=212+2H2O.
(1)根据表格,对比①②的数据,可以看出温度不一样,其它条件都一样,所以实验①②是探究温度对反应速率的影响;实验①③是探究反应物浓度对该反应速率的影响,所以此时两个实验中H2SO4溶液应当不相等,所以选择0.2mol/L硫酸,
故答案为:0.2mol/L硫酸;温度;
(2)探究不同条件对O2+4I-+4H+=212+2H2O反应速率的影响,淀粉遇碘变蓝色,实验中应先向一定体积的KI溶液中滴加淀粉溶液,然后再加入稀硫酸,在酸性条件下发生氧化还原反应生成碘,可根据颜色的变化判断反应速率,应记录的内容是溶液从无色变为蓝色所需的时间,
故答案为:C;溶液从无色变为蓝色所需的时间;
(3)淀粉与碘水作用显蓝色,加入氢氧化钾,若蓝色不褪色,说明溶液中溶液I2和KOH不反应,即验证假设2碱性弱,I2和KOH不反应,
故答案为:碘水;1mol/L KOH溶液;蓝色不褪色.
点评 本题主要考查浓度、温度对反应速率的影响,注意掌握温度、浓度、压强等对反应速率的影响,旨在考查学生灵活运用基础知识解决实际问题的能力,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 28gC2H4和CO的混合气体中含有的分子数为NA | |
| B. | 28gN2和6gH2充分反应,生成NH3的分子数为2NA | |
| C. | 标准状况下,11.2LO2参加反应转移的电子数一定为2NA | |
| D. | 0.1molFeCl3完全水解转化为氢氧化铁胶体,生成0.1NA个胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,当有大量晶体析出时停止加热,用余热使水蒸发 | |
| B. | 蒸馏操作中冷凝管的冷却水应下进上出 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 浓硫酸的稀释可以在量筒中进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10ml质量分数为98%的H2SO4,用10ml水稀释后,H2SO4的质量分数大于49% | |
| B. | 配制0.1mol/L的Na2CO3溶液480mL,需用500mL容量瓶 | |
| C. | 制备Fe(OH)3胶体时,将饱和FeCl3溶液滴入沸水中,边加热边搅拌,直到得到红褐色溶液 | |
| D. | 向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2、和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
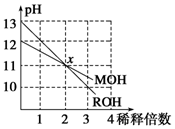 MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示.下列叙述中正确的是( )| A. | MOH和ROH都是强碱 | |
| B. | 稀释前,ROH=10MOH | |
| C. | 常温下pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性 | |
| D. | 在x点,M+=R+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2的溶解度最小 | |
| B. | Ca(OH)2的溶解度最小 | |
| C. | AgCl的溶解度最小 | |
| D. | 同一温度下Ksp越大的溶解度也越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
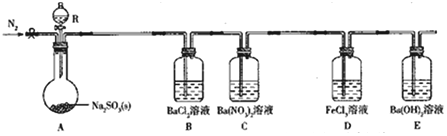
| 实验步骤 | 实验现象及结论 |
| 取少量C中反应后溶液于试管中,加入铜粉(或BaCl2溶液) | 若铜粉溶解,溶液变蓝色(或无沉淀),则猜想2正确;若铜粉不溶解(或产生白色沉淀),则猜想1正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com