
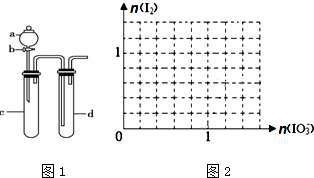
分析 (1)根据在氧化还原反应中,氧化剂的氧化性强于氧化产物,故要实验证明氧化性;KMnO4>Cl2>Br2,需用KMnO4将Cl2氧化出,用Cl2将Br2氧化出,据此分析;根据反应来分析现象;由于氯气、溴蒸汽有毒,故应有尾气处理;
(2)还原性HSO-3>I-,首先发生反应:2IO3-+6HSO3-═2I-+6SO42-+6H+,HSO3-反应完毕,继续加入KIO3,由于氧化性IO-3>I2,再发生反应:IO3-+6H++5I-=3H2O+3I2,由反应可知,可知NaHSO3完全反应需要3mol×$\frac{2}{6}$=1molKIO3,而n(I2)达到最大值时,由IO3-+6H++5I-=3H2O+3I2可知,此时共加入1.2molKIO3,生成I2为0.2mol×3=0.6mol,以此来解答;
(3)根据MnO2和盐酸的反应和氯气与KOH溶液的反应,类推反应;
(4)H2O2与Ca(OH)2作用形成酸式盐为Ca(HO2)2,同时生成水.
解答 解:(1)根据在氧化还原反应中,氧化剂的氧化性强于氧化产物,故要实验证明氧化性;KMnO4>Cl2>Br2,需用KMnO4将Cl2氧化出,用Cl2将Br2氧化出,故a中应放浓盐酸,c中放KMnO4溶液,通过KMnO4能将浓盐酸中的Cl-氧化为Cl2可证明氧化性KMnO4>Cl2;d中放KBr溶液,通过Cl2与KBr溶液反应置换出Br2可以证明氧化性Cl2>Br2,
由于c中有氯气生成,即有黄绿色气体产生,在d中氯气将KBr溶液氧化为单质溴,溶液变为棕黄色.由于氯气、溴蒸汽有毒,故应有尾气处理装置.
故答案为:浓盐酸;KBr溶液;c中有黄绿色气体产生,d中溶液变为棕黄色;无尾气处理装置;
(2)还原性HSO-3>I-,首先发生反应:2IO3-+6HSO3-═2I-+6SO42-+6H+,HSO3-反应完毕,继续加入KIO3,由于氧化性IO-3>I2,再发生反应:IO3-+6H++5I-=3H2O+3I2,由反应可知,可知NaHSO3完全反应需要3mol×$\frac{2}{6}$=1molKIO3,而n(I2)达到最大值时,由IO3-+6H++5I-=3H2O+3I2可知,此时共加入1.2molKIO3,生成I2为0.2mol×3=0.6mol,则图象为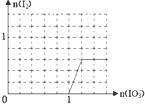 ,故答案为:
,故答案为: ;
;
(3)①由二氧化锰和浓盐酸的反应可知MnO2和HSCN反应的化学方程式为:MnO2+4HSCN(浓)=Mn(SCN)2+(SCN)2↑+2H2O;
故答案为:MnO2+4HSCN(浓)=Mn(SCN)2+(SCN)2↑+2H2O;
②由Cl2+2KOH=KCl+KClO+H2O可知,(CN)2的化学性质和卤素很相似,则(CN)2与KOH(aq)反应的化学方程式为(CN)2+2KOH=KCN+KCNO+H2O,离子方程式为(CN)2+2OH-=CN-+CNO-+H2O;
故答案为:(CN)2+2OH-=CN-+CNO-+H2O;
(4)H2O2为二元酸,其第一步电离方程式为H2O2?H++HO2-,则H2O2与Ca(OH)2作用形成酸式盐为Ca(HO2)2,同时生成水;
故答案为:Ca(HO2)2.
点评 本题考查化学反应方程式的书写,明确信息及离子的还原性与反应的关系即可解答,(2)中注意优先氧化为学生解答的难点,题目难度中等.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:选择题
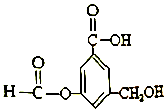
| A. | A 与金属钠完全反应时,两者反应的物质的量之比为1:3 | |
| B. | lmolA最多能与5mol氢气发生反应,反应类型是加成反应 | |
| C. | 1molA与足量碳酸氢钠溶液反应,生成CO2的物质的量为2mol | |
| D. | A既能与羧基反应,又能与醇反应,还能发生水解反应和缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
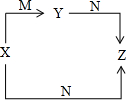 X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )
X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )| A. | X只是钠 | B. | Y只是Na2O | C. | Z只是NaOH | D. | M可能是O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| CO | H2O | H2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的还原性依次增强,热稳定性依次减弱 | |
| B. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| C. | ⅠA金属元素是同周期中金属性最强的元素 | |
| D. | P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com