
分析 (1)先计算出反应过程中硫酸铜的物质的量变化,然后结合反应计算出参加反应的铁的物质的量,再根据m=nM计算出参加反应的铁的质量;
(2)根据质量守恒定律可知反应后硫酸亚铁的物质的量,然后根据c=$\frac{n}{V}$计算出反应后溶液中硫酸亚铁的浓度.
解答 解:(1)反应后恰好硫酸铜减少的物质的量为:n(CuSO4)=(2mol/L-1.6mol/L)×0.05L=0.02mol,
根据反应Fe+CuSO4═Cu+FeSO4可知,消耗0.02molFe的物质的量为:n(Fe)=n(CuSO4)=0.02mol,
所以参加反应的铁皮的质量为:56g/mol×0.02mol=1.12g,
答:参与反应的铁皮的质量为1.12g;
(2)参加反应的Fe的质量为0.02mol,根据质量守恒可知反应后溶液中硫酸亚铁的物质的量为0.02mol,
则反应后溶液中硫酸亚铁的物质的量浓度为:$\frac{0.02mol}{0.05L}$=0.4mol/L,
答:反应后溶液中硫酸亚铁的浓度为0.4mol/L.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | MgCl2、Na2SO4、K2SO4 | B. | KCl、Na2SO4、NaCl | ||
| C. | NaCl、Na2SO4、K2SO4 | D. | KCl、Na2SO4、K2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
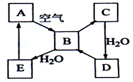 如图表示某固态单质A(淡黄色)及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A(淡黄色)及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 被誉为“百年新药”的阿司匹林的有效成分是乙酰水杨酸,其结构简式如图所示,下列关于乙酰水杨酸的说法中,不正确的是( )
被誉为“百年新药”的阿司匹林的有效成分是乙酰水杨酸,其结构简式如图所示,下列关于乙酰水杨酸的说法中,不正确的是( )| A. | 可用于治疗胃酸过多 | B. | 分子式为C9H8O4 | ||
| C. | 能与乙醇发生酯化反应 | D. | 能与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的最高正化合价为+6 | |
| B. | 元素原子的最外层只有一个电子 | |
| C. | 原子核外各电子层的电子数均达到饱和 | |
| D. | 其最高价氧化物溶于水是强酸,且有气态氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com