
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O26SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________________________________________________________________________;
从腐蚀废液回收得到金属铜,还需要的试剂是________。
 (3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________________________________________________________________________。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________________________________________________________________________。
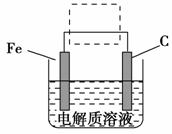
(4)钢铁的电化腐蚀原理如图所示,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在图中虚线框内作出修改,并用箭头标出电子流动方向。
解析 (1)反应中FeS2中的Fe和S失电子发生氧化反应,O2得电子,8 mol O2得到的电子物质的量为32 mol,即为该反应中转移的电子物质的量。(2)回收铜的过程中,Fe3+将Cu氧化为Cu2+,再利用铁将铜置换出来,为除去过量的铁粉可以加入适量稀盐酸或稀硫酸。(3)Fe3+水解导致溶液呈酸性,在酸性废水中H+抑制了Fe3+的水解。(4)电化学防护,可以是原电池原理,也可以是电解原理,故使铁与外加电源的负极相连作阴极即可有效防止钢铁腐蚀。
答案 (1)32 (2)2Fe3++Cu===2Fe2++Cu2+ 铁粉、稀盐酸(稀硫酸)
(3)酸性废水抑制Fe3+的水解,使其不能生成有吸附作用的Fe(OH)3胶体
(4)


科目:高中化学 来源: 题型:
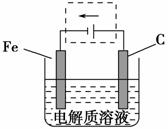
以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。

A.燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
D.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.HClO2 →ClO2+Cl2+H2O(未配平), 1 mol HClO2分解时转移电子的物质的量为1 mol
B.标准状况下,14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA
C.与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+
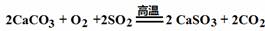
| |
查看答案和解析>>
科目:高中化学 来源: 题型:
要除去铜屑中的少量铁屑。某同学设计了以下两个实验方案:
①加适量CuSO4溶液搅拌过滤—→洗涤
②加适量稀H2SO4溶液搅拌过滤—→洗涤
(1)写出两个实验方案中有关反应的离子方程式:
①__________________________________________________;
②__________________________________________________。
(2)以上两个实验方案中,你愿意选择的是_________________________________。
理由是__________________________________________________
__________________________________________________。
(3)你是否有更简便的方法?写出你的做法。
查看答案和解析>>
科目:高中化学 来源: 题型:
把22.4 g铁粉完全溶解于某浓度的硝酸中,如反应只收集到0.3 mol NO2和0.2 mol NO,下列说法正确的是 ( )。
A.反应后生成的盐只为Fe(NO3)3
B.反应后生成的盐只为Fe(NO3)2
C.反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为1∶3
D.反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是 ( )。
A.Na2O2中阴、阳离子的个数比为1∶1
B.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C.Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D.Na2O2的漂白原理与SO2的漂白原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示。
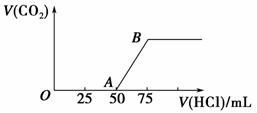
(1)写出OA段所发生反应的离子方程式:________________________________________________________________________。
(2)NaOH在吸收CO2后,所得溶液的溶质为________________________________________________________________________,
其物质的量浓度之比为________。
(3)产生的CO2体积(标准状况下)为________________________________________________________________________。
(4)原NaOH溶液的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(2)相同体积、相同pH值的盐酸和醋酸
①加入足量的Zn,在丙图中画出H2体积的变化图像

单位时间内,________产生的H2多,反应停止时,______产生的H2多。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学想利用图示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物。
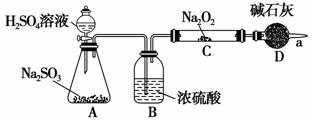
测得反应前C管的质量为m1 g,反应后C管的质量为m2 g,反应后装置D质量增加了n g。请分析:
Ⅰ.装置B的作用_________________________________________________;
装置D的作用_________________________________________________。
Ⅱ.如何检验反应中是否有O2生成______________________________________。
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3,假设2:只有Na2SO4
假设3: ______________________________________________。
(1)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:将C中的固体配成溶液,加Ba(NO3)2溶液,得到白色沉淀,加足量稀硝酸,沉淀不溶解。得出结论:产物是Na2SO4。
该方案是否合理________(填“是”或“否”),理由是__________________________________________________________________
________________________________________________________________________。
(2)若假设1成立,某同学以反应前后C管的质量差(m2-m1)g为依据推断生成Na2SO3的质量为(m2-m1)×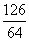 g。老师提示推算不合理,请你分析其中的缘由,________。
g。老师提示推算不合理,请你分析其中的缘由,________。
(3)若假设2成立,则参加反应的Na2O2的物质的量为________mol(列计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com