
����Ŀ����ѧʵ��������ͼ��ʾװ����ȡ�����屽������д���пհס�
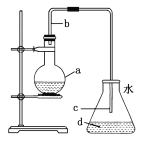
(1)����ƿa��װ���Լ��DZ��������м������b��������������һ�ǵ��������Ǽ���________�����á�
(2)��Ӧ�������ڵ���c���¿ڸ������Թ۲쵽�������֣��������ڷ�Ӧ���ɵ�________��ˮ�������γɵġ�
(3)��Ӧ��Ϻ�����ƿd�е���AgNO3��Һ����________���ɡ�
(4)��Ӧ��Ϻ���ƿa�е�Һ�嵹��ʢ����ˮ���ձ�����Թ۲쵽�ձ��ײ���________ɫ������ˮ��Һ�塣�����ܽ���________�Ĵ��屽��
(5)д����ƿa�з�����Ӧ�Ļ�ѧ����ʽ��____________________��
���𰸡�(1)�������� (2)HBr
(3)����ɫ����(��AgBr����) (4)�� ��
![]()
��������(1)����b��������������һ�ǵ�����������������(�������ܡ�������)��
(2)�а������֣�����Ϊ��Ӧ���ɵ�HBr��ˮ�������γɵ�СҺ�Ρ�
(3)����ƿd�еμ�AgNO3��Һ������dz��ɫ�������ɣ����ӷ���ʽΪAg����Br��===AgBr����
(4)�ձ��ײ��к�ɫ������ˮ��Һ�壬������Ϊ�屽���ܽ��������塣���屽Ϊ��ɫҺ�壬�ܶȱ�ˮ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
ʵ���� | HA���ʵ��� Ũ��(mol��L��1) | NaOH���ʵ��� Ũ��(mol��L��1) | ����� Һ��pH |
�� | 0.1 | 0.1 | pH��9 |
�� | c | 0.2 | pH��7 |
�� | 0.2 | 0.1 | pH<7 |
�����Ҫ��ش�
��1���������������c________ (ѡ��������������С��������������)0.2�����Һ������Ũ��c(A��)��c(Na��)�Ĵ�С��ϵ��______________________________________��
��2���Ӣ���ʵ����������˵��HA�ĵ���̶�________(ѡ��������������С��������������)NaA��ˮ��̶ȣ��û����Һ������Ũ���ɴ�С��˳����_____________________________��
��3������ʵ�����û����Һ����ˮ�������c(OH��)��____________mol��L��1��д���û����Һ��������ʽ�Ľ��(���������Ƽ���)��c(Na��)��c(A��)��________mol��L��1�� c(OH��)��c(HA)��________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Mg2C3�Ľṹ��CaC2���ƣ��ɴ˿ɶ϶�Mg2C3��ˮ��Ӧ�IJ�����(����)
A. Mg(OH)2��CH��CH B. MgO��CH��CH
C. Mg(OH)2��CH3CH=CH2 D. Mg(OH)2��CH3C��CH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.5molNa2SO4�к���Na+����Ŀ�ǣ� ��
A.3.01��1023B.6.02��1023C.0.5D.1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ü�������NO2��Ⱦ�����о���CH4+2NO2 ![]() N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���
N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���
��� | �¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
�� | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
�� | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | �� | 0.15 |
����˵����ȷ����
A. �����У�0~20min�ڣ�NO2�Ľ�������Ϊ0.0125 mol��L-1��min-1
B. ��ʵ�����ݿ�֪ʵ����Ƶ��¶�T12
C. 40minʱ��������T2Ӧ�������Ϊ0.18
D. 0��10min�ڣ�CH4�Ľ������ʢ�>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���22.4L HCl��ȫ����1Lˮ�У�ˮ���ܶȽ���Ϊ1g/mL������Һ���ܶ�Ϊ�� g/cm3����>1������Һ�����ΪV mL�����ʵ���������Ϊw�����ʵ����ʵ���Ũ��Ϊc mol/L��������������ȷ���ǣ�������
��w=![]() ��100%�� ��c=1molL��1�� ����������Һ���ټ���V mLˮ��������Һ��������������0.5w�� ��������Һ�к���NA��HCl���ӣ�
��100%�� ��c=1molL��1�� ����������Һ���ټ���V mLˮ��������Һ��������������0.5w�� ��������Һ�к���NA��HCl���ӣ�
A. ȫ�� B. �٢ۢ� C. �٢� D. ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W�����ڱ��е����λ����ͼ��ʾ������WԪ�ص�ԭ�ӽṹʾ��ͼΪ![]() ��
��
W | X | Y |
Z |
��ش��������⣺
��1��ZԪ����Ԫ�����ڱ��е�λ����___________��
��2��X��Y��Z����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ___________��Ԫ�ط��ű�ʾ����
��3��X��Z��W����Ԫ�ص�����������Ӧˮ�����������ǿ����___________���û�ѧʽ��ʾ����
��4���õ���ʽ��ʾWY2���γɹ��̣�___________��
��5��д��W������Ũ���ᷴӦ�Ļ�ѧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��������Ԫ�أ�Xԭ�ӵ������������Ǵ�����������һ�룬Yλ��X��ǰһ���ڣ��������ֻ��һ�����ӣ���X��Y�γɵĻ�����Ļ�ѧʽ�ɱ�ʾΪ�� ��
A.XY
B.XY2
C.XY4
D.X2Y3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�
(1)Ǧ�����ڷŵ�ʱ�����ĵ�ط�ӦʽΪ��Pb��PbO2��2H2SO4===2PbSO4��2H2O��
�����缫��ӦʽΪ______________��
(2)FeCl3��Һ�����ڸ�ʴӡˢ��·ͭ�壬����2FeCl3��Cu===2FeCl2��CuCl2�������˷�Ӧ��Ƴ�ԭ��أ������õ缫����Ϊ_____________������·��ת��0.2 mol����ʱ����ʴͭ������Ϊ_____________g��
(3)����Ƭ��ͭƬ�õ���������һ�����Ũ�����У�һ������ռ���Һ�У��ֱ��γ���ԭ��أ���������ԭ����У������ֱ�Ϊ______________��
A����Ƭ��ͭƬ B��ͭƬ����Ƭ C����Ƭ����Ƭ
(4)ȼ�ϵ����һ�ָ�Ч�������ѺõĹ���װ�ã���ͼ�ǵ����Ϊϡ������Һ������ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺

������ȼ�ϵ�ص��ܷ�Ӧ��ѧ����ʽ�ǣ�________________��
�ڵ�ع���һ��ʱ���������Һ��Ũ��_____________(���������С�����䡱)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com