
下列叙述正确的是
| A.加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B.常温下由水电离出的H+与OH-的浓度积为10-20mol2·L-2的溶液中可能大量共存的离子组:Na+、S2-、Cl-、CO32- |
| C.向FeI2溶液中通入过量Cl2的离子方程式:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32- |
B
解析试题分析:A、加入铝粉能产生H2的溶液可能为强酸性或强碱性溶液,若为强酸性,酸性条件下Fe2+与NO3-发生氧化还原反应不能大量共存;若为强碱性,NH4+、Fe2+不能大量共存,A不正确;
B、常温下由水电离出的H+与OH-的浓度积为10-20 mol2·L-2的溶液,说明该溶液中水的电离平衡被抑制,因此溶于可能为酸性或碱性溶液,若为酸性,S2-、CO32-不能大量共存;若为碱性,可以共存,B正确;
C、因还原性Fe2+<I-,因此Cl2先氧化I-,再氧化Fe2+,所以当氯气过量时反应的离子方程式应为2Fe2++4I-+3Cl2===2Fe3++2I2+6Cl-,C不正确;
D、向Ca(ClO)2溶液中通入少量CO2时的生成物是碳酸钙沉淀和次氯酸,D不正确,答案选B。
考点:考查离子共存以及离子方程式的正误判断


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:单选题
常温下,下列各组微粒在指定溶液中一定能大最共存的是
| A.由水电离的c(H+)=1×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B.pH=1的溶液中:K+、Cr2O72-、SO42-、CH3CHO |
| C.加石蕊呈蓝色的溶液中:Na+、K+、AlO2-、NO3- |
| D.通入足量CO2后的溶液中:NH4+、Na+、C6H5O-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
往含0.2mol NaOH和0.1mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为6.72L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)( )
A. B. C. D.
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是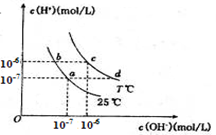
| A.a点对应的无色溶液中能大量存在:Fe3+、Na+、Cl-、SO42- |
| B.b点对应的溶液中能大量存在:NH4+、Ca2+、AlO2-、I- |
| C.c点对应的溶液中能大量存在:Na+、Ba2+、Cl-、CO32- |
| D.d点对应的溶液中能大量存在:Na+、K+、SO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式中,不正确的是
| A.将氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| B.AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| C.FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子在指定溶液中能大量共存的是 ( )
A.滴入酚酞显红色的溶液:Na+、Al3+、SO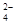 、Cl- 、Cl- |
B.滴入KSCN显红色的溶液:Na+、Cu2+、Br-、SO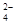 |
C.c( Fe2+)= 1mol·L-l的溶液:H+、Na+、Cl-、NO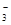 |
D.加入铝粉能产生大量H2的溶液:Na+、K+、Cl-、HCO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列表示对应化学反应的离子方程式不正确的是
| A.FeCl3溶液与Cu的反应:Cu+2Fe3+=Cu2++2Fe2+ |
| B.向NaClO溶液中加入浓盐酸:ClO-+Cl-+2H+=Cl2↑+ H2O |
| C.用氨水溶解Cu(OH)2:Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O |
| D.向NH4HCO3中滴加少量的NaOH溶液:NH4++OH-=NH3·H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在水溶液中能大量共存的一组离子是
| A.HCO3-、H+、NO3-、Na+ | B.Na+、Cu2+、OH-、SO42- |
| C.Mg2+、H+、AlO2-、SO42- | D.NH4+、K+、Br-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com