
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。
反应Ⅰ:CO(g)+2H2(g) ![]() CH3OH(g),△H1
CH3OH(g),△H1
反应Ⅱ:CO2(g)+3H2(g) ![]() CH3OH(g)+ H2O(g),△H2
CH3OH(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
温度 | 250℃ | 300℃ | 350℃ |
K | 2.0 | 0.27 | 0.012 |
(1)在一定条件下将2 molCO和6molH2充入2L的密闭容器中发生反应I,5min后测得c(CO)=0.4 mol/L,计算此段时间的反应速率(用H2表示)___________ mol/(L·min)。
(2)由表中数据判断△H1_____0(填“>”、“<”或“=”)反应,C02(g)+H2(g)![]() CO(g)+H20(g) △H3=____(用△H1和△H2表示)。
CO(g)+H20(g) △H3=____(用△H1和△H2表示)。
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是_________(选字母)。
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K=_________;保持恒温恒容的条件下将反应Ⅱ的平衡体系各物质浓度均增加一倍,则化学平衡_________(填“正向”、“逆向”或“不”)移动,平衡常数K____(填“变大”、“变小”或“不变”)。
【答案】 0.24 < △H2 - △H1 b C(CH3 OH)C(H2 O)/ C(C O2)C3(H2) 正向 不变
【解析】(1)、CO浓度变化量为2mol/2L0.4mol/L=0.6mol/L,故v(CO)=0.6mol/L÷5min=0.12mol/(Lmin),速率之比等于化学计量数之比,故v(H2)=2v(CO)=2×0.12mol/(Lmin)=0.24mol/(Lmin),故答案为:0.24。
(2)、由表中数据可知,随温度升高平衡常数K减小,说明温度升高,平衡逆向进行,所以正向是放热反应,即△H1<0。
反应Ⅰ:CO(g)+2H2(g)CH3OH(g) △H1
反应Ⅱ:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H2
根据盖斯定律ⅡⅠ得到CO2(g)+H2(g)CO(g)+H2O(g),则△H3=△H2△H1,故答案为:<;△H2△H1。
(3)、a.充入CO,使体系总压强增大,平衡向正反应移动,但CO的转化率降低,故a错误;b.将CH3OH(g)从体系中分离,平衡向正反应方向移动,CO转化率增大,故b正确;
c.充入He,使体系总压强增大,但各物质的浓度不变,平衡不移动,CO转化率不变,故c错误;d.使用高效催化剂,平衡不移动,CO的转化率不变,故d错误。故答案为:b。
(4)反应Ⅱ:CO2(g)+3H2(g)CH3OH(g)+H2O(g)的平衡常数k= C(CH3 OH)C(H2 O)/ C(C O2)C3(H2),保持恒温恒容,将反应Ⅱ的平衡体系中各物质浓度均增加一倍,相当于增大压强,平衡向气体体积减小的方向移动即正向移动;平衡常数仅与温度有关,所以平衡常数K不变。故答案为:C(CH3 OH)C(H2 O)/ C(C O2)C3(H2);正向;不变。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】现有三组混合液:①乙酸乙酯和乙酸钠溶液;②乙醇和丁醇;③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是( )
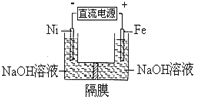
A. 铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+
B. 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C. 若隔膜为阴离子交换膜,则OH-自右向左移动
D. 电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图I是化学实验室中常用制备、干燥气体的部分仪器装置。某学校同学利用中学常用试剂及仪器设计下列实验。

(1)甲同学利用Cu片和浓硝酸在图I装置中制备并收集干燥的NO2气体,
请完成下列问题:
①图I中仪器A的名称_____________;②收集NO2的方法___________;
③B中发生反应的离子方程式为_______________。
④将收集满NO2的烧瓶倒扣入装满水的水槽中,假设溶质不扩散,烧瓶内溶质的物质的量浓度为__________(假设此时为标准状况)。
(2)乙同学利用图I装置制取氨气和氧气的混合气体,并且利用图II装置验证氨的某些性质。A中加入浓氨水,C中加入碱石灰,E内放置催化剂(铂石棉),按气流方向连接各仪器a→b→c→h。请完成下列问题:

①B中加入的固体物质是___________(写出该物质的电子式)。
②实验中观察到E内有红棕色气体出现,证明氨气具有_____性。
③E中发生反应的化学方程式为____________,______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C12H15ClO3)为含多种官能团的芳香族化合物,其结构简式如图所示(其中虚线框内为未知部分的结构),A可发生如下转化(其中部分产物已略去)。
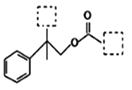
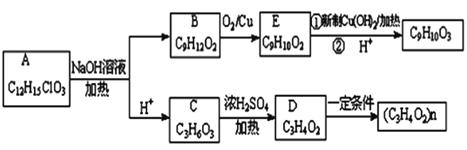
已知:D能使溴的CCl4溶液褪色;B不能与FeCl3溶液发生显色反应,1molB最多能与2mol金属钠反应;C的催化氧化产物不能发生银镜反应。请回答下列问题:
(1)写出E中含氧官能团的名称____________。
(2)写出A的可能的一种结构简式___________。
(3)写出反应类型:C→D_________;B→E__________。
(4)写出E与新制Cu(OH)2反应的化学方程式_____________。
(5)E有多种同分异构体,满足下列条件的同分异构体有_______种,写出其中任意一种同分异构体的结构简式____________。(任写一种)
①含有苯环且苯环上只有一个取代基 ②分子结构中含有甲基 ③能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】张青莲是我国著名的化学家,1991年他准确测得In的相对原子质量为114.818,被国际相对原子质量委员会采用为新的标准值.这是相对原子质量表中首次采用我国测定的相对原子质量值.则下列关于 ![]() In的说法中,错误的是( )
In的说法中,错误的是( )
A.![]() In原子核外有49个电子
In原子核外有49个电子
B.![]() In原子核内有49个中子
In原子核内有49个中子
C.![]() In原子核内质子数和中子数之和等于其质量数,为115
In原子核内质子数和中子数之和等于其质量数,为115
D.![]() In是In元素的一种核素
In是In元素的一种核素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com