
Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) ΔH=-27.6 kJ·mol-1
2Fe(s)+3CO2(g) ΔH=-27.6 kJ·mol-1
3Fe2O3(s)+CO(g)![]() 2Fe3O4(s)+CO2(g) ΔH=-58.6 kJ·mol-1
2Fe3O4(s)+CO2(g) ΔH=-58.6 kJ·mol-1
Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g) ΔH=+38.1 kJ·mol-1
3FeO(s)+CO2(g) ΔH=+38.1 kJ·mol-1
不用查表,计算下列反应的ΔH:FeO(s)+CO(g)![]() Fe(s)+CO2(g)
Fe(s)+CO2(g)
解析:将上列方程式重新排列和乘上有关计量数:
(1)3Fe2O3(s)+9CO(g)![]() 6Fe(s)+9CO2(g) ΔH=3×(-27.6) kJ·mol-1=-82.8 kJ·mol-1
6Fe(s)+9CO2(g) ΔH=3×(-27.6) kJ·mol-1=-82.8 kJ·mol-1
(2)2Fe3O4(s)+CO2(g)![]() 3Fe2O3(s)+CO(g) ΔH=+58.6 kJ·mol-1
3Fe2O3(s)+CO(g) ΔH=+58.6 kJ·mol-1
(3)6FeO(s)+2CO2(g)![]() 2Fe3O4(s)+2CO(g) ΔH=2×(-38.1) kJ·mol-1=-76.2 kJ·mol-1
2Fe3O4(s)+2CO(g) ΔH=2×(-38.1) kJ·mol-1=-76.2 kJ·mol-1
将(1)(2)(3)式相加得:6FeO+6CO![]() 6Fe+6CO2
6Fe+6CO2
则反应:FeO+CO![]() Fe+CO2的ΔH为:
Fe+CO2的ΔH为:
ΔH=(ΔH1+ΔH2+ΔH3)/6=[(-82.8 kJ·mol-1)+58.6 kJ·mol-1+(-76.2 kJ·mol-1)]/6=-16.73 kJ·mol-1


科目:高中化学 来源: 题型:



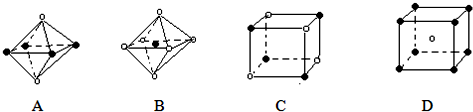

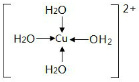

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 序号 | 分解水的过程 | 平衡常数 | T=2500K | T=3000K |
| A | H2O(g)?HO(g)+H(g) | K1 | 1.34×10-4 | 8.56×10-3 |
| B | HO(g)?H(g)+O(g) | K2 | 4.22×10-4 | 1.57×10-2 |
| C | 2H(g)?H2(g) | K3 | 1.52×103 | 3.79×10 |
| D | 2O(g)?O2(g) | K4 | 4.72×103 | 7.68×10 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
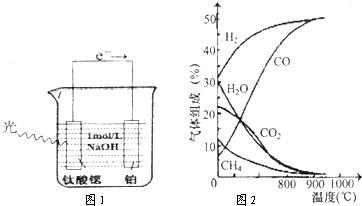
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
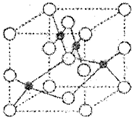
查看答案和解析>>
科目:高中化学 来源: 题型:
| +4 |
| Xe |
| +6 |
| Xe |
| +6 |
| Xe |
| c(H+)×c(F-) |
| c(HF) |
查看答案和解析>>
科目:高中化学 来源:惠安惠南中学2007届高三第一学期期末考试化学试卷-新人教 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com