
【题目】二氧化碳在石油开采、人工降雨、消防、有机合成等领域有着广泛的应用。
(1)甲醇是重要的化工原料。利用合成气(CO、CO2、H2)在催化剂作用下合成甲醇,已知反应相关的化学键键能数据如下:
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(KJ/mol) | 436 | 343 | 803 | 465 | 413 |
写出CO2和H2在催化剂作用下生成CH3OH(g)和H2O(g)的热化学方程式________
(2)CH4超干重整CO2的催化转化原理示意图如图所示:
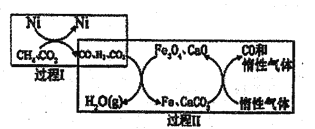
①过程Ⅰ,生成1molH2时吸收123.5kJ热量,其热化学方程式是_______
②过程Ⅱ,实现了含然物种与含碳物种的分离,生成H2O(g)的化学方程式是________
【答案】 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH=-63kJ/mol CH4(g)+CO2(g)
CH3OH(g)+H2O(g)ΔH=-63kJ/mol CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH=+247.0kJ/mol
2CO(g)+2H2(g)ΔH=+247.0kJ/mol ![]()
【解析】(1)该反应的化学方程式为![]() ,反应中生成
,反应中生成![]() 时,
时,![]() 、
、![]() 断键要吸收的能量
断键要吸收的能量![]() ,
,![]() 、
、![]() 成键释放的能量
成键释放的能量![]() ,
,![]() ,热化学方程式为
,热化学方程式为![]() 。
。
(2)①过程Ⅰ,生成1molH2时吸收123.5kJ热量,据图可知该反应的热化学反应方程式为:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH=+247.0kJ/mol
2CO(g)+2H2(g)ΔH=+247.0kJ/mol
②由过程Ⅱ的转化关系看,混合气体中H2将Fe3O4还原为铁,反应的方程式为,实现了含然物种与含碳物种的分离,生成H2O(g)的化学方程式是 ![]()


科目:高中化学 来源: 题型:
【题目】KMnO4是一种氧化剂,实验室常用KMnO4和浓盐酸反应制备Cl2。下图是制备NaClO溶液的装置图。

完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO4的____(选填“氧化性”、“还原性”)。
(2)高锰酸钾溶于水的电离方程式为___________,它属于________(选填“强电解质”、“弱电解质”、“非电解质”)。
(3)高锰酸钾与浓盐酸制备氯气的方程式如下,标出电子转移的方向和数目________,并填空。2KMnO4 + 16HCl(浓)→2KCl + 5Cl2+ 2MnCl2+ 8H2O,反应中被氧化的元素是 ______,在标准状态下生成5.6 L的氯气,转移的电子数为__________________。
(4)B装置中饱和食盐水的作用是 ___________________________________________,D装置中NaOH的作用是 ________________________________________________。
(5)实验操作过程中可调节__________________________以控制A装置中产生Cl2的气流,C装置需控制反应温度在0~5℃,实验中可将C装置放入 __________________中。
(6)除去Cl2中混有的水蒸气和氯化氢气体,选用的药品及顺序正确的是_____________。
A.水、碱石灰 B.饱和食盐水、浓硫酸
C.无水氯化钙、饱和食盐水 D.烧碱溶液、浓硫酸
测定KMnO4纯度可用标准Na2S2O3(式量-158)溶液进行滴定,反应离子方程式为:8MnO4-+5S2O32-+14H+→10SO42-+8Mn2++7H2O。
(7)用已经准确称量过的Na2S2O3固体配制250 mL 0.1000 mol/L标准Na2S2O3溶液,供选择的仪器有:①玻璃棒 ②分液漏斗 ③胶头滴管 ④250 mL容量瓶 ⑤烧杯
⑥烧瓶,必须选用的有__________
A.②③④ B.①③④⑤ C.③④⑤⑥ D.①②④
(8)取某KMnO4(式量-158)产品0.600 g,酸化后用0.1000 mol/L标准Na2S2O3溶液进行滴定,反应最终消耗Na2S2O3溶液20.00 mL,则该KMnO4产品的纯度是_________(保留三位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2(g)+3H2(g)![]() 2NH3(g)ΔH=-92.4kJ/mol起始反应物为N2和H2物质的量之比为1:3,且总物质的量不变,在不同压强和濫度下,反应达到平衡时体系中NH3的物质的量分数如下表:
2NH3(g)ΔH=-92.4kJ/mol起始反应物为N2和H2物质的量之比为1:3,且总物质的量不变,在不同压强和濫度下,反应达到平衡时体系中NH3的物质的量分数如下表:
温度 物质的量分数 压强 | 400℃ | 450℃ | 500℃ | 600℃ |
20MPa | 0.387 | 0.274 | 0.189 | 0.088 |
30MPa | 0.478 | 0.359 | 0.260 | 0.129 |
下列说法正确的是
A. 体系中NH3的物质的量分数越大,则正反应速率越大
B. 反应达到平衡时,N2和H2的转化率之比均为1
C. 反应达到平衡时,放出的热量均为92.4kJ
D. 600℃,30MPa下反应达到平衡时,生成NH3的物质的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的密闭反应器中,只发生两个反应:
a(g) + b(g) ![]() 2c(g) △H1<0 x(g) + 3y(g)
2c(g) △H1<0 x(g) + 3y(g) ![]() 2z(g) △H2 >0
2z(g) △H2 >0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
A. 等压时,通入惰性气体,c的物质的量不变
B. 等压时,通入z气体,反应器中温度升高
C. 等容时,通入惰性气体,各反应速率不变
D. 等容时,通入z气体,y的物质的量浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)厨房中有下列用品:
A. 食盐 B. 小苏打 C. 纯碱 D. 食醋(主要成分为CH3COOH)。
①纯碱的化学式是___________;
②主要成分属于酸式盐的是___________(填序号);
③水溶液呈碱性的是___________(填序号);
④醋酸在水中的电离方程式是______________________。
(2)选择下列实验方法或操作分离物质,请将实验方法的序号填在横线上 (填序号)。
A. 萃取 B. 过滤 C. 蒸馏 D. 加热
①除去粗盐溶液中的泥沙___________;
②利用自来水制取蒸馏水___________;
③从碘水中提取碘___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O==HClO+HSO3-
B. 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合: Al3++2SO42-+2Ba2++4OH- =2BaSO4+AlO2-+ 2H2O
C. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
D. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H+ +2I-=2Fe2+ +I2 +3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。

(1)装置A制取氯气,该反应的化学方程式:___________。
(2)装置C中发生复分解反应制取SO2,该反应的化学方程式:___________。
(3)为验证SO2和Cl2发生了反应,小组同学又继续如下实验。
①甲同学认为若SO2和Cl2反应,生成了Cl-,只要检验到生成的Cl-即可,甲取适量B中样品于试管中,向其中滴加少量___________溶液,有白色沉淀生成。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得到正确结论。洗气瓶中盛有试剂的名称是___________。
③丙同学认为按乙同学的建议改进实验也不合理,理由是:___________。
④丙同学取溶液X于试管中,加入少量反应后B中的溶液,生成大量白色沉淀,得出正确结论:SO2与Cl2同时通入水中,可以发生反应。溶液X是_________(填选项序号)。
a. BaCl2溶液 b. Ba(OH)2溶液 c. 氯水 d. 石蕊溶液
SO2与Cl2同时通入水中反应的化学方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )

A. 所含原子数相等 B. 气体密度相等C.气体质量相等 D.摩尔质量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com