
| A. | m=4 | B. | a=b | C. | a<$\frac{b}{2}$ | D. | m<3 |
分析 甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,压强与物质的量成正比,X、Y的物质的量为2倍的关系,若平衡不移动,b=2c,现b>2c,则加压平衡正向移动,以此来解答.
解答 解:甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,压强与物质的量成正比,X、Y的物质的量为2倍的关系,若平衡不移动,b=2c,现b>2c,则加压平衡正向移动,
所以2+1>m,则m≤2,m等于2或1,
又热化学反应中2molX与1molY完全反应放出akJ热量,向密闭容器甲中通入2mol X和1mol Y,不能完全转化,放出的热量bkJ<akJ,因转化率不知,则无法确定a、b的关系,
故选D.
点评 本题考查化学平衡的计算及热化学反应中物质的量与热量的关系,明确b>2c时平衡移动的方向是解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有白色沉淀生成 | |
| B. | 有红棕色沉淀生成 | |
| C. | 没有沉淀生成 | |
| D. | 既有红褐色沉淀生成又有无色气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
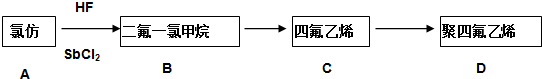
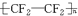 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减少对大气的污染 | B. | 降低成本 | ||
| C. | 防止石油短缺 | D. | 加大发动机的动力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 | |
| B. | 在任何条件下都不能发生Cu+H2SO4═CuSO4+H2↑反应 | |
| C. | 浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 | |
| D. | 二氧化氮与水反应的离子方程式是3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
 ,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;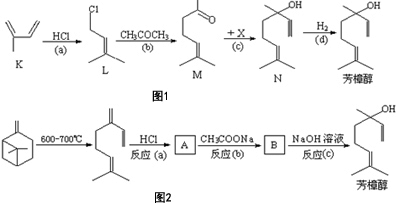
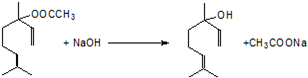 ,.
,.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com