
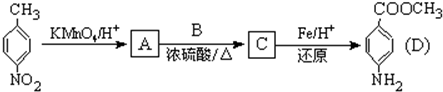
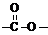 结构的基团的C的所有同分异构体的结构简式:
结构的基团的C的所有同分异构体的结构简式: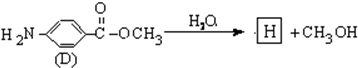
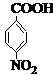 ,A与B反应得到C,C发生还原反应得到D,结合D的结构可知,A与甲醇在浓硫酸作用下发生酯化反应得到C,最后将C硝基还原即等氨基,则B为CH3OH,C为
,A与B反应得到C,C发生还原反应得到D,结合D的结构可知,A与甲醇在浓硫酸作用下发生酯化反应得到C,最后将C硝基还原即等氨基,则B为CH3OH,C为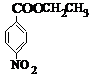 ;
;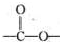 结构的基团,说明含有酯基或羧基,据此确定其结构;
结构的基团,说明含有酯基或羧基,据此确定其结构;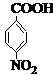 ,A与B反应得到C,C发生还原反应得到D,结合D的结构可知,A与甲醇在浓硫酸作用下发生酯化反应得到C,最后将C硝基还原即等氨基,则B为CH3OH,C为
,A与B反应得到C,C发生还原反应得到D,结合D的结构可知,A与甲醇在浓硫酸作用下发生酯化反应得到C,最后将C硝基还原即等氨基,则B为CH3OH,C为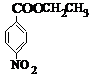 ,故答案为:
,故答案为: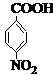 ;CH3OH;
;CH3OH;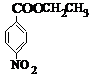 ;
;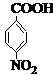 与甲醇发生酯化反应,也属于取代反应,故答案为:酯化反应(或取代反应);
与甲醇发生酯化反应,也属于取代反应,故答案为:酯化反应(或取代反应);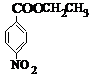 ,用核磁共振氢谱可以证明化合物C中含有4种氢处于不同的化学环境,故答案为:4;
,用核磁共振氢谱可以证明化合物C中含有4种氢处于不同的化学环境,故答案为:4;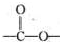 结构的基团,说明含有酯基或羧基,符合条件的同分异构体为:
结构的基团,说明含有酯基或羧基,符合条件的同分异构体为: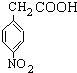 、
、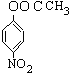 、
、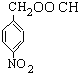 ,
,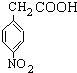 、
、 、
、 ;
; ,其水解反应的化学方程式为:
,其水解反应的化学方程式为: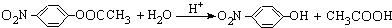 ,
,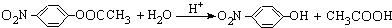 ;
;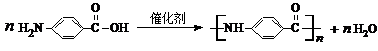 ,故答案为:
,故答案为: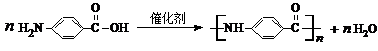 .
.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
| A、ω2<ω1<2ω2 |
| B、ω1>2ω2 |
| C、ω2>ω1>2ω2 |
| D、ω1=2ω2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
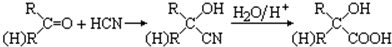
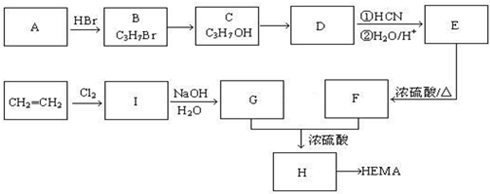
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
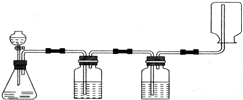 某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )
某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )| A、锌和盐酸反应制取氢气 |
| B、二氧化锰和浓盐酸反应制取氯气 |
| C、碳酸钙和盐酸反应制取二氧化碳 |
| D、过氧化钠和水反应制取氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
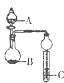
| A、若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
| B、若A为浓硫酸,B为木炭,C中盛有硅酸钠溶液,则C中出现白色浑浊 |
| C、若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色 |
| D、若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀不溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com