
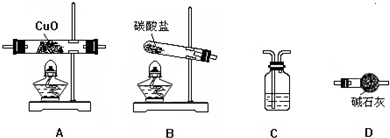
 N2+3Cu+3H2O.备选仪器装置如下(装置内所发生的反应是完全的).
N2+3Cu+3H2O.备选仪器装置如下(装置内所发生的反应是完全的).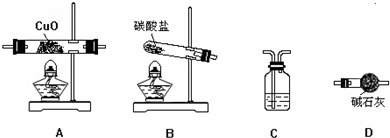
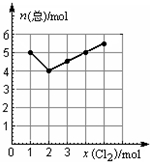
 N2+3Cu+3H2O
N2+3Cu+3H2O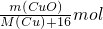
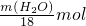
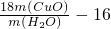
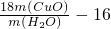 ;
;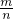 结合方程式进行计算;
结合方程式进行计算;

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| 18m(CuO) |
| m(H2O) |
| 18m(CuO) |
| m(H2O) |
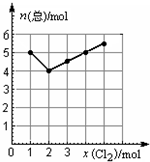
查看答案和解析>>
科目:高中化学 来源:西城区一模 题型:填空题
| ||
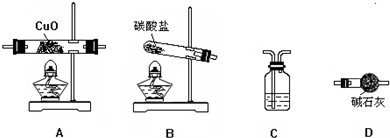
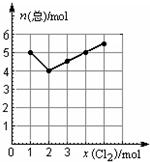
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2009年北京市西城区高考化学一模试卷(4月份)(解析版) 题型:填空题
 N2+3Cu+3H2O.备选仪器装置如下(装置内所发生的反应是完全的).
N2+3Cu+3H2O.备选仪器装置如下(装置内所发生的反应是完全的).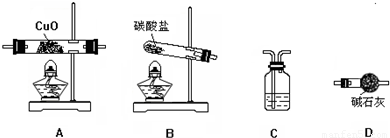
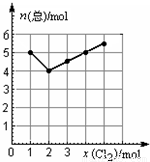
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com