
 1,2-二溴乙烷是常用的有机合成中间体,某小组用如图装置合成1,2-二溴乙烷.
1,2-二溴乙烷是常用的有机合成中间体,某小组用如图装置合成1,2-二溴乙烷.| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1,2二溴乙烷 | 131.4 | 2.18 | 微溶 |
| 溴 | 58.8 | 3.12 | 微溶 |
| 乙醇 | 78.5 | 0.79 | 溶 |
分析 合成1,2-二溴乙烷.装置B:乙醇在浓硫酸作用下加热到170℃发生消去反应生成乙烯和水,装置C:平衡气压,装置D:用氢氧化钠溶液除去SO2、CO2,装置E:溴与乙烯发生反应,装置F:尾气吸收,
(1)根据浓硫酸密度大于乙醇和乙酸,且混合过程中浓硫酸放出大量热进行解答;乙醇沸点低,使用冰水浴降温可防止乙醇挥发;
(2)为防止暴沸,装置B中还应加入碎瓷片,B装置产生乙烯气体,装置C有竖直的玻璃管,与空气相通,可以稳定装置中的压强,起安全瓶作用,溴易挥发,E中试管里加水的目的是防止溴挥发;
(3)乙烯和溴水发生了加成反应,溴水褪色;为防止倒吸,反应结束时正确的操作是断开DE之间的导管,再停止加热;
(4)根据洗涤操作选择玻璃仪器;
(5)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,8.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为9.4g,根据产率=$\frac{实际产量}{理论产量}$×100%计算;
(6)通入乙烯气体速率过快,影响乙烯吸收,未除掉乙烯中的杂质影响产品质量,溴、1,2-二溴乙烷挥发需液封防止挥发.
解答 解:(1)浓硫酸密度较大,混合过程会放出大量热,所以正确操作方法为:先向试管中加入乙醇,然后边振荡边慢慢加入浓硫酸,乙醇沸点低,温度高易挥发,使用冰水浴降温可防止乙醇挥发,
故答案为:先加乙醇,再加浓硫酸;防止乙醇挥发;
(2)乙醇沸点低,加热易沸腾,装置B中还应加入碎瓷片引入汽化中心,防止暴沸,B装置产生乙烯气体,装置C有竖直的玻璃管为安全管,与空气相通,当C压力过大时,安全管中液面上升,使C瓶中压力稳定,并能发现装置是否堵塞,能平衡气压,液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,所以E中试管里加水的目的是防止溴、产物1,2-二溴乙烷挥发,
故答案为:碎瓷片;平衡气压;防止溴、产物1,2-二溴乙烷挥发;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以判断生成1,2-二溴乙烷反应结束的方法是E中试管里的液体变为无色,为防止倒吸,反应结束时正确的操作是断开DE之间的导管,再停止加热,
故答案为:E中试管里的液体变为无色;断开DE之间的导管,再停止加热;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层,所以需要的玻璃仪器为:分液漏斗、烧杯,
故答案为:分液漏斗、烧杯;
(5)根据反应方程式CH2=CH2+Br2→BrCH2CH2Br可知,8.0g的溴和足量的乙醇制备1,2-二溴乙烷的质量为9.4g,所以产率=$\frac{实际产量}{理论产量}$×100%=$\frac{6.3g}{9.4g}$×100%≈67%,
故答案为:67%;
(6)a.乙烯通入溴时迅速鼓泡,部分乙烯未被吸收,产量偏低,故选;
b.装置D:用氢氧化钠溶液除去SO2、CO2,实验室没有装置D,二氧化硫能与溴水反应生成硫酸和氢溴酸,产量偏低,故选;
c.液溴有强挥发性,反应放热,产物1,2-二溴乙烷也能的挥发,水可以起保护作用,减少产品挥发引起的损失,若去掉装置E烧杯中的水,产量偏低,故选;
d.装置F尾气吸收,其中的NaOH溶液用水代替,无影响,故不选.
故答案为:abc.
点评 本题考查了1,2-二溴乙烷的实验室制备和性质的检验,明确制备原理是解题关键,注意掌握乙醇、乙烯性质及检验方法,题目难度中等.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 水果表面喷洒驱虫剂不招苍蝇 | B. | 自来水使用氯制剂以杀菌消毒 | ||
| C. | 牛肚用甲醛浸泡使其口感更好 | D. | 生豆芽时用植物生长激素提高产量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 | |
| ① | ${\;}_{19}^{40}$K | 19 | 21 | 19 | 40 |
| ② | 3818Ar | 18 | 20 | 18 | 38 |
| ③ | 3216S2- | 16 | 16 | 18 | 32 |
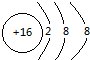 Mg2+
Mg2+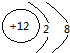 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C |
| D |
| A. | C的非金属性最强,可分别与A、E元素形成离子化合物 | |
| B. | 元素D可形成三种常见的酸,且酸根离子均能促进水的电离 | |
| C. | C单质可以从D、E组成的化合物的水溶液中置换出D | |
| D. | 离子半径由大到小的顺序为:D>E>A>B>C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
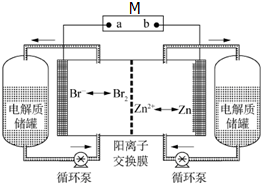 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环流动.左侧电极为惰性电极.放电时M是用电器,充电时M是外电源.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环流动.左侧电极为惰性电极.放电时M是用电器,充电时M是外电源.下列说法不正确的是( )| A. | 锌溴液流电池总反应为:Zn+Br2═ZnBr2 | |
| B. | 放电时右侧电池电极发生氧化反应,电流从a极经用电器流向b极 | |
| C. | 放电时Zn2+从右侧经阳离子交换膜移向左侧,左侧电解质储罐中的离子总浓度增大 | |
| D. | 充电时左侧溴离子浓度下降,左侧电池电极连接电源的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
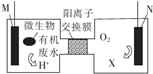 为解决淀粉厂沸水中BOD严重超标的问题,有人设计了电化学降解法,如图是利用一种微生物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
为解决淀粉厂沸水中BOD严重超标的问题,有人设计了电化学降解法,如图是利用一种微生物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )| A. | N极是负极 | |
| B. | 负极的电极反应为(C6H10O5)n]+7nH2O-24ne-═6nCO2↑+24nH+ | |
| C. | 物质X是OH- | |
| D. | 该装置工作时,H+从右侧经阳离子交换膜转向左侧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa与O2反应得到32g固体产物,钠失去电子数为NA | |
| B. | 用1mL0.1mol•L-1FeCl3溶液制得的氢氧化铁胶体所含胶粒数为10-4NA | |
| C. | 12g金刚石中含有的共价键数为2NA | |
| D. | 标准状况下,22.4LCH4中含有的碳原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
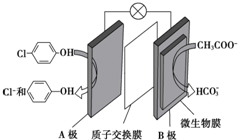 含乙酸钠和对氯酚(
含乙酸钠和对氯酚(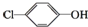 )的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )
)的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )| A. | 电极B是负极 | |
| B. | 质子从A极移向B极 | |
| C. | B极的电极反应式:CH3COO--8e-+4H2O═2HCO3-+9H+ | |
| D. | 处理后的废水pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
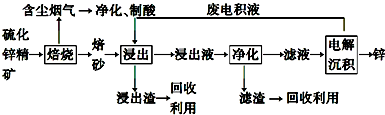
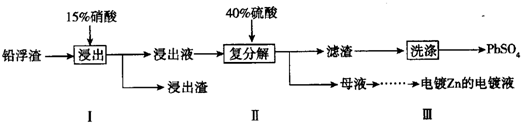
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com