
【题目】下列关于摩尔质量叙述中正确的是( )
A. 1 mol CO 的质量是 28 g·mol-1 B. 硫酸根离子的摩尔质量是 98 g
C. Cl2 的摩尔质量是 71 g·mol D. NaCl 的相对分子质量是 58.5 g·m
科目:高中化学 来源: 题型:
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)写出实验室制备氨气的化学方程式:______________________________ ;氨的水溶液显弱碱性,其原因为__________________________(用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”) ;若加入少量的明矾,溶液中的NH的浓度________(填“增大”或“减小”) 。
(2)硝酸铵加热分解可得到N2O和H2O。250 ℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为________________________________,平衡常数表达式为________;若有1 mol硝酸铵完全分解,转移的电子数为________mol。
(3)将pH=12的氨水和pH=2的盐酸等体积混合后溶液呈______性。
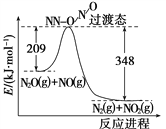
(4)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500 ℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和__________。
(2)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。

① A中固体充分加热较长时间后,通入氮气,目的是__________________________。
②为验证A中残留物是否含有FeO,需要选用的试剂有____________(填字母)。
A.KSCN溶液 B.稀硫酸
C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有________气体生成,若含有该气体,观察到的现象为_______________________________________。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为b mol,C中沉淀物质的量为a mol,则b________________(填“大于”“小于”或“等于”)a。
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为___________________________________________(用离子方程式表示)。
(3)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O的含量,某实验小组做了如下实验:
测定原理:MnO![]() +Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
+Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
测定步骤:步骤一:准确称量20.00 g硫酸亚铁铵晶体,配制成100 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,用0.100 0 mol·L-1 KMnO4溶液滴定至终点,重复两次,平均消耗KMnO4溶液16.00 mL。
①如何判断滴定终点?________________________;
②产品中(NH4)2Fe(SO4)2·6H2O的质量分数为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、C60和石墨 C、35Cl和37Cl
D、 E、乙醇和乙二醇
E、乙醇和乙二醇
①互为同位素的是______________;②互为同系物的是____________;
③互为同素异形体的是_____________;④互为同分异构体的是______________;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是__________。
(2)选择合适的药品鉴别下列有机物组合(将试剂名称或者化学式填在横线上)
① CCl4和苯_____________ ②己烷和己烯_____________ ③苯和甲苯______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.强酸和强碱一定是强电解质,不论其水溶液浓度大小,都能完全电离
B.强电解质溶液的导电能力一定比弱电解质强
C.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
D.强电解质不一定都是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A. 在多电子的原子里,能量高的电子通常在离核近的区域内活动
B. 核外电子总是先排在能量高的电子层上,由里向外逐层排布
C. 两种微粒,若核外电子排布完全相同,则其化学性质不一定相同
D. 微粒的最外层只能是8个电子才稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知An+、B(n-1)+、C(n+1)+、D(n+1)-都有相同的电子层结构,A、B、C、D的原子半径由小到大的顺序是( )
A. C>D>B>A B. D >C> A>B C. B>A>C>D D. A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷与氯气以物质的量之比1∶3混合,在光照下得到的产物:①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4,正确的是 ( )
A、只有① B、只有②
C、①②③的混合物 D、①②③④的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的性质决定物质反应的现象,关于钠与水反应的现象和钠的下列性质无关的是( )
A. 钠的熔点较低 B. 钠的密度小于水
C. 钠的硬度较小 D. 钠的还原性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com