
| A、在中和热测定的实验中,将氢氧化钠溶液和盐酸混合反应后的最高温度作为末温度 |
| B、检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,先用稀硫酸进行酸化,再加人AgN03溶液进行检验 |
| C、为了加快过滤速度以及得到较干燥的硅酸白色胶状沉淀可以采用抽滤的方法 |
| D、用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在固定相中分配的更多 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
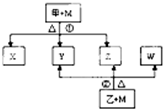 A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大.B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等.X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成.元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙).转化关系如图(反应条件略去).请回答下列问题:
A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大.B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等.X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成.元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙).转化关系如图(反应条件略去).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HF、H2O的沸点比HCl、H2S的沸点高很多 |
| B、正戊烷的沸点比新戊烷的沸点高 |
| C、H2O的沸点比FH的沸点高 |
| D、HF、HCl、HBr、HI的稳定性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4L |
| B、44.8L |
| C、小于22.4L |
| D、小于44.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期表含元素最多的族是第ⅢB族 |
| B、元素周期表有18个族 |
| C、短周期是指第一、二、三、四周期 |
| D、第ⅠA族的元素全部是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
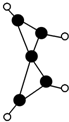 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )| A、该分子的分子式为C5H4 |
| B、该分子中碳原子的化学环境有2种 |
| C、1mol X在一定条件下可与2mol H2发生反应 |
| D、该分子中只有C-C键,没有C═C键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3溶液使酚酞变红:CO32-+H2O?H2CO3+OH- |
| B、向Ba(OH)2溶液中加入稀H2SO4溶液:Ba2++SO42-═BaSO4↓ |
| C、向NaHCO3溶液中加入稀盐酸溶液:CO32-+2H+═H2O+CO2↑ |
| D、NH4Cl溶液显酸性:NH4++H2O?NH3?H2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究控制汽车尾气成为保护环境的重要任务.汽车内燃机工作时发生反应:
研究控制汽车尾气成为保护环境的重要任务.汽车内燃机工作时发生反应:| 温度(℃) | c(氨水)(mol/L) | 电离常数 | 电离度(%) | c(OH-)(mol/L) |
| 0 | 16.56 | 1.37×10-5 | 9.098 | 1.507×10-2 |
| 10 | 15.16 | 1.57×10-5 | 10.18 | 1.543×10-2 |
| 20 | 13.63 | 1.71×10-5 | 11.2 | 1.527×10-2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com