
如图所示,在不同的电解质溶液中可以组 成不同的电池。
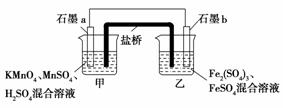
(1)①当电解质溶液为稀硫酸时,Fe电极是______(填“正”或“负”)极,其电极反应式为____________________________________________________________。
②当电解质溶液为NaOH溶液时,Al电极是______(填“正”或“负”)极,其电极反应式为________________________。
(2)若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______(填“正”或“负”)极,其电极反应式为________________________。
科目:高中化学 来源: 题型:
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。
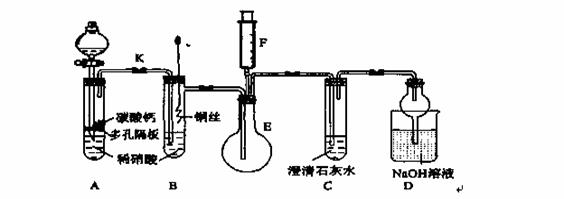
请回答有关问题:
(1)设计装置A的目的是
为达到此目的,应进行的操作是
(2)在完成(1)中的操作后,将装置B中铜丝插入稀硝酸,并微热之,观察
到装置B中的现象是
B中反应的离子方程式为:
(3)装置E和F的作用是
为实现此作用,其操作方法是
(4)装置D的作用是
查看答案和解析>>
科目:高中化学 来源: 题型:
为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一星期,下列对实验结束时现象描述不正确的是( )。
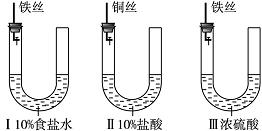
A.装置Ⅰ左侧的液面一定会上升
B.左侧液面装置Ⅰ比装置Ⅱ的低C.装置Ⅱ中的铁钉腐蚀最严重
D.装置Ⅲ中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
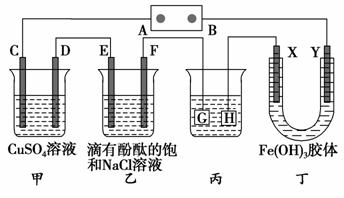
请回答:
(1)B极是电源的________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明____________________,在电场作用下向Y极移动。
(2)若甲 、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______________。
、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______________。
(3)现用丙装置给铜件镀银,则H应该是________(填“镀层金属”或“镀件”),电镀液是 ________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温常压下在1 L水中可溶解40 L NO2,NO2能与NaOH溶液发生反应:2NaOH+2NO2===NaNO3+NaNO2+H2O。以下各种尾气吸收装置中,不适合吸收NO2气体的是( )
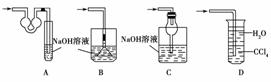
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com