
����������ĵ���ƽ�ⳣ�����±���
���� | HCOOH | HClO | H2CO3 | H2SO3 |
����ƽ�ⳣ��(25 ��) | Ka��1.77 ��10��4 | Ka��4.0 ��10��8 | Ka1��4.3��10��7 Ka2��4.7��10��11 | Ka1��1.54��10��2 Ka2��1.02��10��7 |
(1)�����¢�0.1 mol��L��1 HCOONa����0.1 mol��L��1 NaClO����0.1 mol��L��1 Na2CO3����0.1 mol��L��1 NaHCO3��Һ��pH�ɴ�С�Ĺ�ϵΪ______________________��
(2)Ũ�Ⱦ�Ϊ0.1 mol��L��1��Na2SO3��Na2CO3�Ļ����Һ�У�SO32-��CO32-��HSO3-��HCO3-Ũ�ȴӴ�С��˳��Ϊ____________________��
(3)����CO2ͨ�뵽������NaClO��Һ�з�����Ӧ�����ӷ���ʽ______________��
(4)�����£�pH��3��HCOOH��Һ��pH��11��NaOH��Һ�������Ϻ���Һ������Ũ���ɴ�С��˳��Ϊ__________________��
����ijС�����ù�ҵ�����ӽ���Ĥ�����ռ��ԭ����������ͼ��ʾװ�õ��K2SO4��Һ��
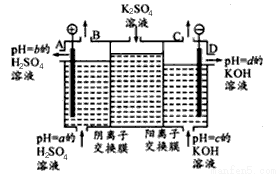
�ٸõ�����ͨ�������ӽ���Ĥ��������_______���>����<����һ����ͨ�������ӽ���Ĥ����������
��ͼ��a��b��c��d�ֱ��ʾ�й���Һ��pH����a��b��c��d��С�����˳��Ϊ _____________��
�۵��һ��ʱ���B������C���ڲ��������������Ϊ______________��
 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017������к�����������ѧ����ĩ���ԣ���ѧ�ڿ�ѧ���ԣ���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�����pH=2�����ᣬ����˵������ȷ����
A. ��Һ��c(H+)=1.0��10-2 mol��L-1
B. ����Һ����ˮ�������c(OH-)=1.0��10-12 mol��L-1
C. ��ˮϡ��100������Һ��pH=4
D. ��������pH=12�İ�ˮ����Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ���˴���������2��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������ȷ����
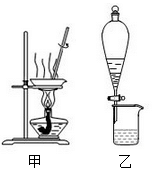
A. ������ƿ������Һʱ����������ˮϴ�ӣ����ô�װ��Һ��ϴ
B. ��ʪ��ĺ�ɫʯ����ֽ������������
C. ��װ�ü��ȷֽ�Al(OH)3����
D. ��װ���ҷ������������ͱ���̼������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��УЭ�����һ��ѧ���ڳ���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ӣ�������Һ�д����������
A. Na+ ��Mg2+ ��Cl- ��SO42- B. Na+ ��Ca2+ ��CO32- ��NO3-
C. Na+ ��H+ ��Cl- ��CO32- D. K+ ��Al3+ ��SO42- ��OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��УЭ�����һ��ѧ���ڳ���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ��100 mL 0.5 mol/L NaCl��Һ��������Cl�����ʵ���Ũ����ͬ����
A. 100 mL 0.5 mol/L MgCl2��Һ B. 200 mL 0.25 mol/L AlCl3��Һ
C. 50 mL 1 mol/L NaCl��Һ D. 25 mL 0.5 mol/L HCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����( )
A. ij���ʵ���Һ����ˮ�������c(H+)��1��10-a mol/L����a��7ʱ�������Һ��pHһ��Ϊ14-a
B. ��ͬ���ʵ���Ũ�ȵ�������Һ�У���NH4Al(SO4)2����NH4Cl����CH3COONH4����NH3��H2O��c(NH4+) �ɴ�С��˳���ǣ���>��>��>��
C. ���ʵ���Ũ����ȵ�H2S��NaHS�����Һ�У�c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. AgCl����Һ�д���ƽ�⣺ AgCl(s)  Ag+(aq)+Cl-(aq)�������м������� NaCl��ĩ��ƽ��������ƶ�����Һ�����ӵ���Ũ�Ȼ��С
Ag+(aq)+Cl-(aq)�������м������� NaCl��ĩ��ƽ��������ƶ�����Һ�����ӵ���Ũ�Ȼ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£�0.01mol/L NaOH��pHΪ10�����¶��½�pH=5��ǿ����Һ��pH=8��ǿ����Һ��Ϻ�pH=7��������Һ����ͼ���Һ�����Ϊ�� ��
A. 1��10 B. 10��1 C. 9��2 D. 2��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���ӱ�ʡ2016-2017ѧ���һ��ѧ�ڿ�ѧ���Ի�ѧ�Ծ� ���ͣ�ѡ����
�谢���ӵ�����ΪNA������˵����ȷ����
A. ���³�ѹ�£�22.4LH2O�к��е���ԭ����Ϊ2NA
B. 17gNH3��18 g H2O�����е�������Ϊ10NA
C. 2.7 g Al��������NaOH��Һ��Ӧ������H2�ķ�����Ϊ0.1NA
D. 1 mol HCl�����еķ�������2L 0.5 mol/L�����е��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���½�����ũ��ʦ��ɽ��ѧ��һ��ѧ��ѧǰ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����������ԭ��Ӧ��
��2FeCl3+2KI=2FeC12+2KCl+I2 ��2FeCl2+Cl2 =2FeCl3
��2KMnO4+16HCI��Ũ��=2KCl+2MnCl2+8H2O+5Cl2��
��ij��Һ����Fe2+��Iһ��Cl�����棬Ҫ��I��������ȥ��������Fe2+��Cl������ɼ�����Լ���
A. Cl2 B. KMnO4 C. FeCl3 D. HCl
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com