
| A. | 两种化合物组成元素相同,且各元素的质量分数也相同,则两者一定是同分异构体 | |
| B. | 分子中有6个碳原子的烃只能形成5个碳碳单键 | |
| C. | 丙烯分子中的所有原子都在同一平面内 | |
| D. | 分子式为C3H6Cl2与C3H2Cl6的有机物所具有的同分异构体数目相同 |
分析 A.组成元素相同,各元素质量分数也相同,最简式相同;
B.有6个碳原子的烃,可形成环状结构;
C.甲烷是正四面体结构;
D.C3H6Cl2可看做C3H2Cl6中的氢原子被氯原子取代,氯原子被氢原子取代.
解答 解:A.组成元素相同,各元素质量分数也相同,最简式相同,如乙炔、苯不是同分异构体,故A错误;
B.有6个碳原子的烃,可形成环状结构,则分子中有6个碳原子的烃最多形成6个碳碳单键,故B错误;
C.丙烯中含有一个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故C错误;
D.C3H6Cl2可看做C3H2Cl6中的氢原子被氯原子取代,氯原子被氢原子取代,同分异构体数目相同,故D正确.
故选D.
点评 本题考查有机物的官能团及结构,为高频考点,把握物质的组成、结构、同分异构体的判断为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
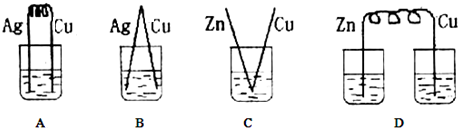
| A. | 三种实验方案都能制得纯净的铜 | |
| B. | 乙方案中加过量铁粉可以将四种阳离子全部还原 | |
| C. | 甲方案中的反应涉及置换、分解、化合、复分解四种反应类型 | |
| D. | 丙方案会产生环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 :1,2-二甲苯.
:1,2-二甲苯. CH3COONH4+H2O+2Ag↓+3NH3.
CH3COONH4+H2O+2Ag↓+3NH3. )与2mol乙醇发生酯化反应的化学方程式:
)与2mol乙醇发生酯化反应的化学方程式: .
. ,可能发生的化学反应除加成反应外,还有取代反应(填一种反应类型).
,可能发生的化学反应除加成反应外,还有取代反应(填一种反应类型).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
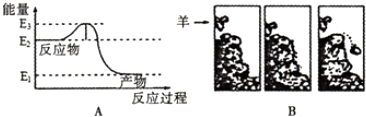
| A. | E2 | B. | E3 | C. | E2-E1 | D. | E3-E2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
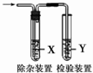 用如图所示装置检验对应气体时,不能达到目的是( )
用如图所示装置检验对应气体时,不能达到目的是( ) | 生成的气体 | 试剂X | 试剂Y | |
| A | 电石与水反应制取的乙炔 | CuSO4 | Br2的CCl4溶液 |
| B | 证明苯与液溴的反应是取代反应而不是加成反应 | 水 | AgNO3溶液 |
| C | CH3CH2Br与NaOH乙醇溶液共热制取的乙烯 | 水 | KMnO4酸性溶液 |
| D | C2H5OH与浓硫酸加热至170℃制取乙烯 | NaOH溶液 | Br2的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C+H20$\frac{\underline{\;\;△\;\;}}{\;}$C0+H2 | B. | H+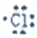 → →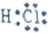 | ||
| C. | H20(1)→H20(g) | D. | CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 用萃取的方法分离汽油和煤油 | |
| C. | 将稀H2SO4与BaCl2的反应设计成原电池 | |
| D. | 将氢气和氧气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com