
| A. | 32g | B. | 48g | C. | 16g | D. | 64g |
分析 2molC在一定量的O2中充分燃烧,生成CO、CO2,其中CO的物质的量为1mol,根据C原子守恒知,生成n(CO2)=n(C)-n(CO)=2mol-1mol=1mol,根据O原子守恒计算消耗氧气物质的量,再根据m=nM计算氧气质量.
解答 解:2molC在一定量的O2中充分燃烧,生成CO、CO2,其中CO的物质的量为1mol,根据C原子守恒知,生成n(CO2)=n(C)-n(CO)=2mol-1mol=1mol,根据O原子守恒得消耗n(O2)=$\frac{n(CO)+2n(C{O}_{2})}{2}$=$\frac{1mol+2×1mol}{2}$=1.5mol,m(O2)=nM=1.5mol×32g/mol=48g,
故选B.
点评 本题考查化学方程式有关计算,为高频考点,侧重考查学生分析计算能力,利用原子守恒分析解答,题目难度不大.


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应右边方框内的产物是OH- | B. | 配平该反应后,H+的化学计量数是8 | ||
| C. | 该反应中氧化产物是CO2 | D. | 该反应电子转移总数是5e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 铜跟稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| C. | 向AlCl3溶液中加入过量的氨水溶液:Al3++3OH-=Al(OH)3↓ | |
| D. | 氯气通入冷的氢氧化钠溶液中 2Cl2+2OH-=3Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤③①⑥⑦ | B. | ④②⑤③①⑥⑦ | C. | ②④⑤③⑥①⑦ | D. | ⑦⑥①③⑤④② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
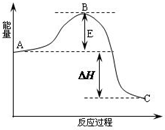 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol•L-1) | 0.10 | a | 0.026 | 0.0065 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
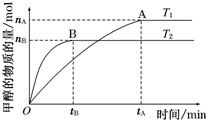 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com