
| A、3.18 g |
| B、2.21 g |
| C、5.28 g |
| D、4.22 g |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、有丁达尔现象 |
| B、一定是悬浊液 |
| C、一定能透过半透膜 |
| D、利用过滤的方法可分离出纳米材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2-酸性氧化物-Na2O2-碱性氧化物 Al2O3-两性氧化物 |
| B、汽油-混合物 胆矾-纯净物 O3-单质 |
| C、纯碱-碱 硫化氢-酸 小苏打-酸式盐 |
| D、液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
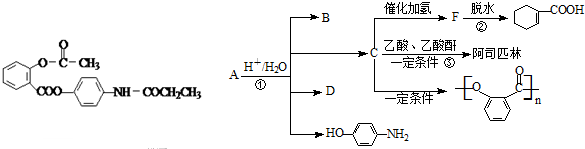
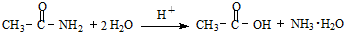
查看答案和解析>>
科目:高中化学 来源: 题型:
 铜属于不活泼金属,但却能被FeCl3溶液腐蚀,请写出其离子反应方程式
铜属于不活泼金属,但却能被FeCl3溶液腐蚀,请写出其离子反应方程式查看答案和解析>>
科目:高中化学 来源: 题型:
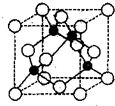 VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com