
��12�֣�ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���塣
��1��XԪ�ط�����
��2��Z��W�γɵ���̬�⻯����ȶ������� �������� ��д��ѧʽ����
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ�����ӷ���ʽΪ ��
��4����X��Y��Z��W����Ԫ����ɵ�һ�����ӻ�����A����֪��1mol A��������NaOHŨ��Һ��Ӧ���ɱ�״����44��8L���塣��A�������ᷴӦ�������壬������������ˮ��Ӧ��д������������ˮ��Ӧ�����ӷ���ʽ ��
��5����X��Y��Z��W��Fe����Ԫ����ɵ�ʽ��Ϊ392�Ļ�����B��1 mol B�к���6mol�ᾧˮ���Ի�����B��������ʵ�飺
a��ȡB����Һ�������ŨNaOH��Һ�����ȣ�������ɫ��������ɫ�̼�����ζ���壻��
һ��ʱ���ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��
b����ȡB����Һ���������BaCl2��Һ������ɫ������������������ܽ⡣
����ʵ��a ��b ��֪B��Һ�к��е�����Ϊ ��
��B�Ļ�ѧʽΪ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 H2SO3��H2SO3
H2SO3��H2SO3 H++HSO3-
H++HSO3- H2SO3��H2SO3
H2SO3��H2SO3 H++HSO3-
H++HSO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
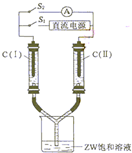 X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�أ���֪����X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ����
X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�أ���֪����X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com