
| 500�� |
| NaOH |
| �ữ |
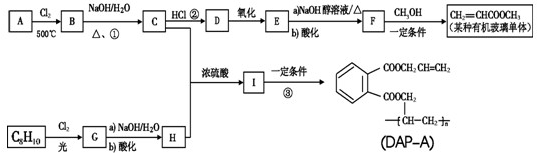
 ����֪IΪ��
����֪IΪ�� ��C��H����I����HΪ
��C��H����I����HΪ ��G������Ϣ��Ӧת����H����GΪ
��G������Ϣ��Ӧת����H����GΪ ������C8H10Ϊ
������C8H10Ϊ ���ݴ˽��н��
���ݴ˽��н�� ����֪IΪ��
����֪IΪ�� ��C��H����I����HΪ
��C��H����I����HΪ ��G������Ϣ��Ӧת����H����GΪ
��G������Ϣ��Ӧת����H����GΪ ������C8H10Ϊ
������C8H10Ϊ ��
�� ��
�� ��
�� ��
��| H2O |
| �� |
| H2O |
| �� |
 ����һ���������ܹ����Ҷ�������������Ӧ���ɸ߷��ӻ������Ӧ����ʽΪ��
����һ���������ܹ����Ҷ�������������Ӧ���ɸ߷��ӻ������Ӧ����ʽΪ�� ��
�� ��
��

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4?14H2O | ||
| B��CH4?8H2O | ||
C��CH4?
| ||
| D��CH4?6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
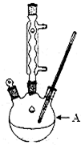
| ��һ�� | �ڶ��� | ������ | ���Ĵ� | |
| �����mL�� | 24.00 | 24.10 | 22.40 | 23.90 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �� | �� | �� | �� | �� |
| ���ϼ� | -4 | -1 | +1 | -4 | -2 |
| A�����ij��������������� |
| B����̬�⻯���ȶ��ԣ������� |
| C�����������������ҵ��⻯���ˮ��Һ��Ӧ |
| D��ԭ�Ӱ뾶��С�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
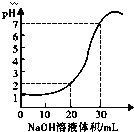 ��ͼΪ10mL x mol?L-1��������y mol?L-1��NaOH��Һ�ζ���ͼ������ͼ���Ƴ�x��y����ֵ���������и����еģ�������
��ͼΪ10mL x mol?L-1��������y mol?L-1��NaOH��Һ�ζ���ͼ������ͼ���Ƴ�x��y����ֵ���������и����еģ�������| A | B | C | D | |
| x | 0.12 | 0.04 | 0.03 | 0.09 |
| y | 0.04 | 0.12 | 0.09 | 0.03 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| NaOH��H2O |
| �� |
| ���� |
| ���� |
 ��1��
��1�� ��һ�������¿ɷ������Ʒ�Ӧ�ٵķ�Ӧ�������л�������������Ľṹ��ʽΪ
��һ�������¿ɷ������Ʒ�Ӧ�ٵķ�Ӧ�������л�������������Ľṹ��ʽΪ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com