
分析 相同条件下体积比等于物质的量比,设平衡时N2O4和NO2混合气体中各物质的量分别为xmol和ymol,混合气体的平均分子质量为57.5,则$\frac{92x+46y}{x+y}$=57.5;
N2O4(g)?2NO2(g),
开始 a 0
转化 n 2n
平衡 a-n 2n
(a-n):2n=x:y,以此来解答.
解答 解:(1)设平衡时N2O4和NO2混合气体中各物质的量分别为xmol和ymol,混合气体的平均分子质量为57.5,则$\frac{92x+46y}{x+y}$=57.5,解得x:y=1:3,即平衡时,混合气体中N2O4与NO2的体积比为1:3,
答:平衡时,混合气体中N2O4与NO2的体积比为1:3;
(2)设充入N2O4气体为a,
N2O4(g)?2NO2(g),
开始 a 0
转化 n 2n
平衡 a-n 2n
(a-n):2n=x:y=1:3,
解得n=0.6a,
N2O4的平衡转化率为$\frac{0.6a}{a}$×100%=60%,
答:N2O4的平衡转化率为60%.
点评 本题考查化学平衡的计算,为高频考点,把握平均相对分子质量的计算、平衡三段法、转化率计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
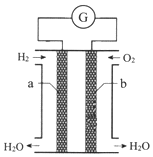 氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )
氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )| A. | a电极是该电池的正极 | |
| B. | 电池工作时,电从a电极流出经导线流向b电极 | |
| C. | 工作一段时间后,电解质溶液碱性减弱 | |
| D. | b极的电极反应式为:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | 铜加入稀硝酸中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 澄清石灰水与过量NaHCO3溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于0.54mol | B. | 小于0.54mol | C. | 等于1.00mol | D. | 大于1.00mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaCl+H2SO4(浓)$\stackrel{加热}{→}$NaHSO4+HCl↑ | |
| B. | 2FeO+4H2SO4(浓) $\stackrel{加热}{→}$Fe2(SO4)3+SO2↑+4H2O | |
| C. | C+2H2SO4(浓) $\stackrel{加热}{→}$CO2↑+2SO2↑+2H2O | |
| D. | 2Al+6H2SO4(浓) $\stackrel{加热}{→}$Al2(SO4)3+3SO2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液与铜反应:Fe3++Cu═Fe2++Cu2+ | |
| B. | 氢氧化铁与稀盐酸反应:OH-+H+═H2O | |
| C. | 钠与水的反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a、b、d均可以与c形成两种或多种二元化合物 | |
| B. | d的原子半径是这些元素中最大的 | |
| C. | a与d形成的化合物可以抑制水的电离 | |
| D. | 常温下,由这四种元素构成的某种盐的溶液pH=4,则水电离出的H+浓度肯定是1×10-4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com