
【题目】中和滴定是化学定量实验之一。某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
(1)在中和滴定的过程中有如下操作:①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤,则在操作过程中正确的顺序是__________________。(写序号)
(2)选用的指示剂是 。(a、石蕊 b、甲基橙)
(3)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的空白处。
滴定次数 | 待测氢氧化钠溶液的体积/ mL | 0.1000 mol/L 盐酸的体积/ mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/ mL | ||
第一次 | 25.00 | |||
第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
(6)请根据上表中数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)= 。
(7)滴定终点的判定依据是 。
【答案】(1)③⑤①②④ (2)b
(3)锥形瓶内溶液颜色的变化 (4)D
(5)0.00 26.10 26.10 (6)0.1044mol/L
(7)溶液恰好由黄色变为橙色,且保持半分钟不褪色(2分)
【解析】
试题分析:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,所以正确的顺序是③⑤①②④;(2)石蕊颜色太深,一般不用,所以答案B;(3)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化;(4)A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液被稀释,浓度减小,造成V(标准)偏大,根据c(待测)=![]() 可知,c(待测)偏大,错误;B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
可知,c(待测)偏大,错误;B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=![]() 可知,测定c(NaOH)无影响,错误;C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
可知,测定c(NaOH)无影响,错误;C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=![]() 可知,c(待测)偏大,错误;
可知,c(待测)偏大,错误;
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)=![]() 可知,c(待测)偏小,正确。(5)起始读数为0.00mL,终点读数为26.10mL,盐酸溶液的体积为26.10mL;(6)根据3组实验,平均消耗V(盐酸)=26.10mL,结合方程式
可知,c(待测)偏小,正确。(5)起始读数为0.00mL,终点读数为26.10mL,盐酸溶液的体积为26.10mL;(6)根据3组实验,平均消耗V(盐酸)=26.10mL,结合方程式
HCl + NaOH = NaCl + H2O,0.0261L×0.1000mol·L-1 = 0.025L×C(NaOH),解得C(NaOH)=0.1044mol·L-1;(7)滴定终点时溶液颜色由黄色突变为橙色,且半分钟内不褪色。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2,可通过二氧化碳甲烷化再利用。
请回答:
⑴已知:2Al2O3(s)=4Al(g)+3O2(g) △H1=3351 kJ·mol-1
2C(s)+O2(g)=2CO(g) △H2=-221 kJ·mol-1
2Al(g) + N2(g)=2AlN(s) △H3=-318 kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是_____,该反应自发进行的条件____________。
(2)在常压,Ru/TiO2催化下,CO2和H2混合气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应I CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
反应II CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2

①下列说法不正确的是_____
A. △H1小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
②350℃时,反应I在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为________(用a、V表示)。
③350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。________

据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用。回答下列问题:
(1)基态磷原子有________种不同能量的电子。
(2)N、P、As电负性由大到小的顺序为 ______ ,它们的氢化物沸点最高的为_______________,原因为___________________________。
(3)NO3- 离子的空间构型为_____,中心原子的杂化方式为_____ ,NO3-离子有多种等电子体,请写出一种_________ 。
(4)钛元素原子核外价电子排布图为____________,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配离子中含有的化学键类型为____________,该配离子的配位数为____________。
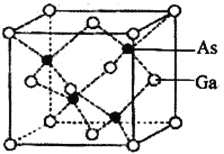
(5)砷化镓晶胞结构如下图。晶胞中距离Ga原子等距且最近的Ga原子有_________个,Ga与周围等距且最近的As形成的空间构型为____________。已知砷化镓晶胞边长为a pm,其密度为ρgcm-3,则阿伏加德罗常数的数值为_____________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1 mol/L的HA溶液中![]() =1010,0.01 mol/L的BOH溶液pH=12。请回答下列问题:
=1010,0.01 mol/L的BOH溶液pH=12。请回答下列问题:
(1)HA是_________(填“强电解质”或“弱电解质”,下同),BOH是__________。
(2)HA的电离方程式是_______________________________________。
其中由水电离出的c(H+)=________mol/L
(3)在加水稀释HA的过程中,随着水量的增加而减小的是_______(填字母)。
A.![]()
B.![]()
C.c(H+)与c(OH-)的乘积
D.c(OH-)
(4)将等体积等物质的量浓度的HA溶液和BOH溶液混合后的溶液呈 性,请用离子方程式解释其原因_____________,混合溶液中各离子浓度由大到小的顺序是 。
(5)常温下pH=12的BOH溶液100mL,加0.01mol/L NaHSO4使溶液的pH为11。(混合溶液体积变化忽略不计),应加_________mL(保留到小数点后一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关。下列说法错误的是
A. 晶体硅是良好的半导体材料,用于制作光导纤维
B. 新型净水剂的制备和应用,进一步提高了饮用水的质量
C. 过氧化钠可用作为制氧剂
D. 深海底层“可燃冰”的试采成功,为其使用开拓了广阔前景
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列有关叙述正确的是
A. CO2的摩尔质量是44
B. NA个SO2分子的质量是64g
C. 1L1mol·L-1Na2SO4溶液中Na+数为NA
D. 9gH2O中氧原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学反应N2(g)+![]() H2(g)
H2(g)![]() NH3(l)的能量变化如图所示,
NH3(l)的能量变化如图所示,

该反应放出的热量为____________________(用代数式表示)
(2)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数为____________。
(3)铅蓄电池是最早使用的充电电池,由Pb、PbO2、稀硫酸构成,该电池工作时,(工作原理:Pb+PbO2+2H2SO4===2PbSO4+2H2O),若电路中转移2mol电子,则负极材料质量的变化量为_________g.
(4)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:该反应中X的平衡转化率为__________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说正确的是( )
A.物质的量就是1摩尔物质的质量
B.1 mol水中含有2 mol氢和1 mol氧
C.1 molH2中含有6.02个氢分子
D.CO2的摩尔质量是44 g/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com