
分析 根据n=$\frac{m}{M}$硫酸物质的量,氧原子物质的量为硫酸的4倍,再根据N=nNA计算氧原子数目;
根据n=$\frac{m}{M}$氧气酸物质的量,根据V=nVm计算氧气体积.
解答 解:24.5g硫酸的物质的量为$\frac{24.5g}{98g/mol}$=0.25mol,则氧原子数目为0.25mol×4×NAmol-1=NA;
48g O2的物质的量为$\frac{48g}{32g/mol}$=1.5mol,在标准状况下氧气的体积为1.5mol×22.4L/mol=33.6L,
故答案为:NA;33.6L.
点评 本题考查物质的量有关计算,比较基础,掌握物质的量为中心的计算公式,有利于基础知识的巩固.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温、同压下,相同质量的气体都占有相同的体积 | |
| B. | 同温、同压下,相同体积的气体都含有相同数目的分子 | |
| C. | 在标准状况下,1 mol水的体积约是22.4 L | |
| D. | 1 mol某气体的体积约为22.4 L,该气体所处的状况一定是标准状况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2既是氧化剂又是还原剂 | |
| B. | NaN3中N元素被还原 | |
| C. | 每生成16molN2转移30mole- | |
| D. | 还原产物与氧化产物质量之比为1:15 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4 Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图甲装置构成锌-铜原电池 | B. | 用图乙装置除去NO2中的NO | ||
| C. | 用图丙装置制备SO2气体 | D. | 用图丁装置制取干燥的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. ①、②、③3个-OH的酸性由强到弱的顺序是:
①、②、③3个-OH的酸性由强到弱的顺序是: .
.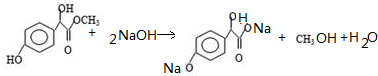 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com