
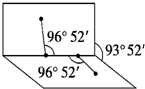
 已知H2O2的结构如图:H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O-H键与O-O键的夹角均为96°52′,试回答:
已知H2O2的结构如图:H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O-H键与O-O键的夹角均为96°52′,试回答: ;
; ;
;

 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
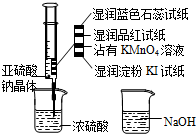 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )| A、蓝色石蕊试纸先变红后褪色 |
| B、NaOH溶液可用于除去实验中多余的SO2 |
| C、湿润淀粉KI试纸未变蓝说明SO2的氧化性强于I2 |
| D、品红试纸、沾有KMnO4溶液滤纸均褪色都能证明SO2的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
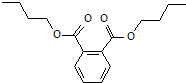
| A、属于芳香族化合物,能溶于水 |
| B、其核磁共振氢谱共有6种吸收峰 |
| C、分子中一定有12个原子位于同一平面上 |
| D、水解得到的酸性产物能与乙二醇发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4L过重氧化氢所含的分子数为NA |
| B、过重氧化氢与过氧化氢的化学性质相似,都既有氧化性又有还原性,还具有酸性 |
| C、过重氧化氢的摩尔质量为38g |
| D、过重氧化氢分子是由极性键形成的非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O2的电子式为 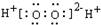 |
| B、4℃时,纯水的pH>7,呈中性 |
| C、100℃、101kPa时,水分子间距:液态>气态 |
| D、101kPa时,相同质量的水在不同状态下的能量:固态>液态>气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲基的电子式: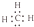 | ||
B、硫原子的原子结构示意图: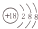 | ||
C、中子数为50,质子数为39的钇(Y)的核素:
| ||
D、间-硝基甲苯的结构简式: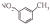 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市五校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列溶液中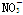 的物质的量浓度最大的是
的物质的量浓度最大的是
A.500 mL 1 mol·L-1的KNO3溶液
B.500 mL 1 mol·L-1的Ba(NO3)2溶液
C.1000 mL 0.5 mol·L-1的Mg(NO3)2溶液
D.1 L 0.5 mol·L-1的Fe(NO3)3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com