
某实验小组用工业上废弃固体(主要成分Cu2S和Fe2O3)混合物制取粗铜和Fe2(SO4)3晶体,设计的操作流程如下:
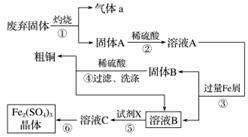
(1)③实验操作中用到的玻璃仪器有________________________________________。
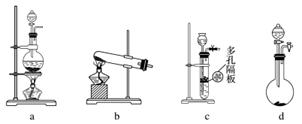
(2)③④操作中会有一种气体生成,若在实验室制备该气体,可选择下列哪些装置________(填字母)。
(3)溶液B在空气中放置有可能变质,如何检验溶液B是否变质:__________________。
(4)溶液B加稀硫酸酸化后加强氧化剂X,试剂X最好选择下列哪种试剂______________(填字母)。
a.Cl2 b.H2O2 c.KMnO4
试剂X在酸性条件下与溶液B反应的离子方程式为________________________。
(5)由溶液C经________、________、过滤等操作得Fe2(SO4)3晶体。
(6)某同学用实验制得的Fe2(SO4)3晶体配制0.1 mol·L-1的Fe2(SO4)3溶液,在称量出Fe2(SO4)3晶体后,溶解该晶体的具体操作为_______________________________________________。
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
下列物质的分类正确的是( )
A.共价化合物——硫酸、纯碱、水
B.分散系——空气、水玻璃、盐酸
C.非电解质——液氯、乙醇、NH3
D.强氧化剂——盐酸、硫酸、硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如下图所示。
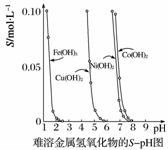
(1)pH=3时溶液中铜元素的主要存在形式是________(写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为______(填字母)。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,______(填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___________________________________。
(4)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的________除去它们(填字母)。
A.NaOH B.FeS C.Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
现代科技的高度快速发展离不开C和Si元素。
(1)写出Si的基态原子核外电子排布式__________________。
(2)从电负性角度分析,C、Si、O元素的非金属活泼性由强至弱的顺序为______。
(3)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为_____,微粒间存在的作用力是_______。
(4)C、Si为同一主族的元素,CO2 、SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成上述π键,而Si、O原子间不能形成上述π键:_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用KClO3和浓盐酸反应也可以制备氯气。某研究性学习小组利用如图所示装置在实验室中制取Cl2并探究其相关性质:
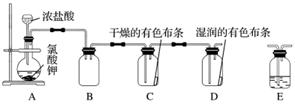
(1)装置A中存在一处错误,请改正这处错误:_________________________________。
(2)写出装置A中发生反应的化学方程式:__________________________________________
________________________________________________________________________。
(3)为了除去氯气中的氯化氢,需要在装置A、B之间添加装置E,装置E中所盛装的试剂为________________。为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为________(填字母)。
a.A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入集气瓶B中,可以观察到的现象是______________________,能检验该反应产物中铁元素价态的试剂是________(填字母)。
a.氯水 b.蒸馏水和铁粉
c.氢氧化钠溶液 d.KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷,并给出了改进措施,该改进措施是________________________________________________________________________
__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
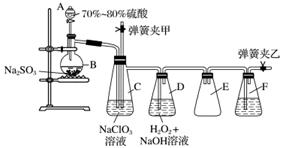
装置C中发生反应:2NaClO3+SO2===2ClO2+Na2SO4(Ⅰ)
装置D中发生反应:2ClO2+H2O2+2NaOH===2NaClO2+2H2O+O2(Ⅱ)
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是________________________。实验开始时,打开A的活塞,两个弹簧夹的开关操作是__________________,F中盛有的液体为________。
(2)装置B中进行的是用硫酸与亚硫酸钠制备二氧化硫的反应,该处使用的是70%~80%的硫酸,而不是98%的浓硫酸或极稀的硫酸,原因是___________________________________。
(3)装置C的作用是________________,装置E的作用是________________。
(4)在碱性溶液中NaClO2比较稳定,所以装置D中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是________。
a.稀盐酸 b.品红溶液 c.石蕊溶液 d.酚酞溶液
(5)一次实验制备中,通过检验发现制备的NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是__________________。检验产物中含有Na2SO3杂质的实验操作和现象是________________________________________________________________________。
(供选择的试剂有:Ba(OH)2溶液、H2O2溶液、AgNO3溶液、品红溶液、H2SO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空
(1)形状大小相同的铁、铝分别与等浓度的盐酸反应生成氢气的速率:铁______铝(填“大于”、“小于”或“等于”)。
(2)对于Fe+2HCl===FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”、“减小”或“不变”)
①升高温度:________;
②增大盐酸浓度:__________;
③增大铁的质量:__________;
④增加盐酸体积:____________;
⑤把铁片改成铁粉:____________;
⑥滴入几滴CuSO4溶液:____________;
⑦加入NaCl固体:____________;
⑧加入CH3COONa固体____________;
⑨加入一定体积的Na2SO4溶液____________。
(3)若把(2)中的稀盐酸改成“稀硝酸”或“浓硫酸”是否还产生H2,为什么?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①参加反应的物质的性质是影响化学反应速率的主要因素
②光是影响某些化学反应速率的外界条件之一 ③决定化学反应速率的主要因素是浓度 ④不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电解质的叙述正确的是( )
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离
C.强极性共价化合物不一定都是强电解质
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com