
����Ŀ��5�ֹ�������A��B��C��D��E�ɱ��в�ͬ������������ɣ����Ǿ�������ˮ��
������ | Na+ | Al3+ | Fe3+ | Cu2+ | Ba2+ |
������ | OH�� | Cl�� | CO32�� | NO3�� | SO42�� |
�ֱ�ȡ���ǵ�ˮ��Һ����ʵ�飬������£�
��A��Һ��C��Һ��Ϻ������ɫ��������ó����м�������ϡHNO3 �� ���������ܽ⣬ʣ���ɫ���壻
��B��Һ��E��Һ��Ϻ�������ɫ������ͬʱ�����������壻
������C��Һ��D��Һ��Ϻ������ɫ����������C��Һ��D��Һ��Ϻ�������
��B��Һ��D��Һ��Ϻ�������
�ݽ�38.4g CuƬͶ��װ������D��Һ���Թ��У�CuƬ���ܽ⣬�ٵμ�1.6molL��1ϡH2SO4 �� Cu���ܽ⣬�ܿڸ����к���ɫ������֣�
��1���ݴ��ƶ�A��C�Ļ�ѧʽΪ��A��C ��
��2��д��������з�����Ӧ�����ӷ���ʽ ��
��3��D��Һ�е���ʯ����Һ�������� �� ԭ�����������ӷ���ʽ˵������
��4�����������Ҫ��CuƬ��ȫ�ܽ⣬���ټ���ϡH2SO4�������mL��
���𰸡�
��1��CuSO4��Ba��OH��2
��2��2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2��
��3����Һ����ɫ��ɺ�ɫ��Al3++3H2O?Al��OH��3+3H+
��4��500
���������⣺5�ֹ�������A��B��C��D��E�ɱ��в�ͬ������������ɣ����Ǿ�������ˮ�������ӹ����֪��һ�����У�Na2CO3��Ba��OH��2 �� ��A��Һ��C��Һ��Ϻ������ɫ��������ó����м�������ϡHNO3 �� ���������ܽ⣬ʣ���ɫ���壬˵������������ͭ�����ᱵ����A��C�ֱ�ΪBa��OH��2��CuSO4�е�һ�֣���B��Һ��E��Һ��Ϻ�������ɫ������ͬʱ�����������壬˵���������������������̼��Ӧ̼���������η���˫ˮ�ⷴӦ��B��E�ֱ�ΪNa2CO3�������е�һ�֣�������C��Һ��D��Һ��Ϻ������ɫ����������C��Һ��D��Һ��Ϻ�������Ϣٿ�֪��CΪBa��OH��2��DΪ���Σ���AΪCuSO4����B��Һ��D��Һ��Ϻ�������Ϣڿ�֪��BΪ���Σ�EΪNa2CO3 �� �ݽ�38.4g CuƬͶ��װ������D��Һ���Թ��У�CuƬ���ܽ⣬�ٵμ�1.6molL��1ϡH2SO4 �� Cu���ܽ⣬�ܿڸ����к���ɫ������֣�D����NO3�� �� ��Ϣۿ�֪DΪAl��NO3��3 �� ������������֪B�к���Cl�� �� ��BΪFeCl3 �� ��1�����ƶ�A��C�Ļ�ѧʽΪCuSO4��Ba��OH��2 �� ���Դ��ǣ�CuSO4��Ba��OH��2����2������ڣ�EΪNa2CO3��Һ��BΪFeCl3��Һ�����߷���˫ˮ�ⷴӦ�����������������Ͷ�����̼�����䷴Ӧ����ʽΪ��2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2����
���Դ��ǣ�2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2������3��DΪAl��NO3��3��Һ��������Һ�����ԣ���Ϊ������ˮ�����������ӣ��� Al3++3H2OAl��OH��3+3H+ �� ��������Һ�е���ʯ����Һ����Һ������ɫ��ɺ�ɫ��
���Դ��ǣ�����ɫ��ɺ�ɫ�� Al3++3H2OAl��OH��3+3H+����4��38.4 g Cu�����ʵ���Ϊ�� ![]() =0.6mol��������з��������ӷ�Ӧ����ʽΪ��3Cu+8H++2NO3��=3Cu2++2NO+4H2O����Ҫ��CuƬ��ȫ�ܽ⣬��Ҫ�����ӵ����ʵ���Ϊ1.6mol�������ټ���ϡH2SO4�������ΪV����1.6mol/L��V��2=1.6mol����V=500mL��
=0.6mol��������з��������ӷ�Ӧ����ʽΪ��3Cu+8H++2NO3��=3Cu2++2NO+4H2O����Ҫ��CuƬ��ȫ�ܽ⣬��Ҫ�����ӵ����ʵ���Ϊ1.6mol�������ټ���ϡH2SO4�������ΪV����1.6mol/L��V��2=1.6mol����V=500mL��
���Դ��ǣ�500��


 ȫ��������ϵ�д�
ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ�١��ڷֱ��ǴӺ���Һ�ij�ֿ�ʯ����ȡ�����Ҫ��Ӧ�� ��2NaI+MnO2+3H2SO4�T2NaHSO4+MnSO4+2H2O+I2
��2NaIO3+5NaHSO3�T2Na2SO4+3NaHSO4+H2O+I2 ��
����˵����ȷ���ǣ� ��
A.������Ӧ��NaHSO4��Ϊ��������
B.��Ԫ���ڷ�Ӧ���б���ԭ���ڷ�Ӧ���б�����
C.�����ԣ�MnO2��SO ![]() ��IO
��IO ![]() ��I2
��I2
D.��Ӧ�١��������ɵ�����I2ʱת�Ƶ�������Ϊ1��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������������ȷ���ǣ�������
A.���³�ѹ�£�22.4L H2���еķ�����ΪNA
B.25�桢101KPaʱ��1mol CO2������ռ�е����ԼΪ22.4L
C.��״���£�4.0g NaOH���е�Na+������Ϊ0.1NA
D.���ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl������Ϊ1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������У�800��ʱ��Ӧ2NO��g��+O2��g��2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO��/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K= �� ��֪��K��300�棩��K��350�棩���÷�Ӧ����Ӧ������ȡ������ȡ����� 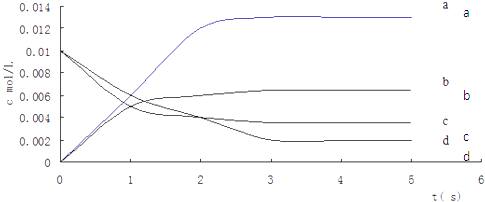
��2��ͼ�б�ʾNO2�ı仯�������� �� ��O2��Ũ�ȱ仯��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v= ��
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d�����������ʵ��ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����( )
A. ̫���ܵ�ؿ��ö������������������Ӧ�������ڻ�������
B. SiO2������������ά
C. Na2SiO3ˮ��Һ�׳�ˮ������������ľ�ķ������𤽺��
D. ������Ͽ���ʹ���˴���ˮ�࣬ˮ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��һ�廷���飨 ![]() ����NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽����
����NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽����
�ף���Ӧ���Һ�е���ϡ�����к�NaOH��Ȼ���ٵ���AgNO3��Һ������dz��ɫ�����������֤����������ȥ��Ӧ��
�ң���Ӧ���Һ�е�����ˮ������Һ��ɫ�ܿ���ȥ�����֤����������ȥ��Ӧ��
������Ӧ���Һ�е�������KMnO4��Һ������Һ��ɫ��dz�����֤����������ȥ��Ӧ��������ȷ���ǣ� ��
A.��
B.��
C.��
D.����ʵ�鷽��������ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ͨ����MnO2��Ũ���ᷴӦ��ȡ�������䷴Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��1���ڸ÷�Ӧ�У�����1mol Cl2���ɣ���������HCl�����ʵ�����mol��ת�Ƶ��ӵ����ʵ�����mol��
��2����ֽ�����˶�����������ϴʱ������ʹ�á�����顱����Ҫ�ɷ������ᣩ�롰84����Һ������Ҫ�ɷ���NaClO�����������ж����¼����Ը�����Ļ�ѧ֪ʶ������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(˫ѡ��)�������������ȷ����( )
A.��ķǽ����Խ�ǿ������ֻ�Ի���̬��������Ȼ��
B.����ڻ�ҩ�е�����ء�̿����Ҫ�õ�����̼��ˮ�Լ����˲���
C.���������ǽ�����Ӧ����Ϊ������
D.1.6 g����6.4 gͭ��Ӧ�ܵõ�8.0 g��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǹ�������κ���������˵����ȷ���� ��������
A.����ʹ�ú���ϴ�Ӽ��������ɫ��Ⱦ
B.����ʹ�÷��ȴ����Ŀ����Ϊ�˼�������
C.�������ɵ���ˮ������������ˮ������
D.�����������ƶ���ȼú��ů������Ϊȼ��ú���ж����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com